ФОТОЭЛЕКТРОННАЯ СПЕКТРОСКОПИЯ
(ФЭС), метод изучения электронного строения в-ва, основанный на явлении
фотоэффекта с использованием УФ излучения. При поглощении фотона атомом среды
испускается электрон (фотоэлектрон), причем энергия фотона hn (n - частота
излучения, h - постоянная Планка) за вычетом энергии связи ЕСВ
электрона передается фотоэлектрону и м. б. измерена как его кине-тич. энергия
Eкин:
Eсв =
hn - Eкин.
Фотоэлектронную спектроскопию и рентгеноэлектронную
спектроскопию иногда объединяют общим названием "электронная спектроскопия".
Разделение между двумя методами условно: при 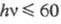 эВ говорят о фотоэлектронной спектроскопии, при больших hn - о рентгеноэлектронной спектроскопии.
эВ говорят о фотоэлектронной спектроскопии, при больших hn - о рентгеноэлектронной спектроскопии.
В фотоэлектронной спектроскопии используют монохроматич.
излучение He(I) или Не(П), энергия фотона соотв. 21,2 и 40,8 эВ; реже применяют
резонансные линии излучения др. инертных газов и монохро-матизир. синхротронное
излучение. Энергетич. спектры фотоэлектронов измеряют в фотоэлектронных спектрометрах,
осн. элементы к-рых - источник излучения, электростатич. анализатор энергии
электронов Eкин и детектор электронов для измерения интенсивности
полос фотоэлектронного спектра, к-рая пропорциональна содержанию соответствующего
элемента в образце. Разрешающая способность (ширина полос) составляет от 10
до 80 мэВ, точность определения Eкин достигает 10-25
мэВ.
Фотоэлектронная спектроскопия позволяет изучать
электронные и колебат. уровни энергии молекул, потенциалы ионизации (как
вертикальные, так и адиабатические), поверхностные эффекты и др. характеристики.
Колебат. структура фотоэлектронных спектров хорошо проявляется у сравнительно
простых двухатомных молекул, к-рые м. б. представлены моделью двух взаимодействующих
точечных масс m1 и m2 [приведенная масса
M= m1m2/(m1 + m2)] с равновесным
расстоянием между ними r (длина связи) и гармонич. силовой постоянной К (см.
Колебательные спектры). Согласно классич. механике, частота колебаний
wи атомных ядер ионизированной молекулы, рассчитываемая по данным
ИК спектров, связана с M и К соотношением: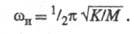
Если фотоэлектрон удаляется
со связывающей мол. орбитали, величина К меньше, а если с разрыхляющей
орбитали -больше, чем значение, к-рое входит в аналогичное соотношение для неионизир.
молекулы, следовательно, фотоэлектронная спектроскопия позволяет установить характер мол. орбиталей,
если сравнить фотоэлектронную частоту 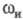 с частотой колебаний
с частотой колебаний 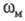 для неионизированной (свободной) молекулы.
для неионизированной (свободной) молекулы.
Значения 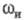 и
и 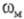 связаны
с адиабатич. (Iа) и вертикальным (Ib)
потенциалами ионизации соотношением:
связаны
с адиабатич. (Iа) и вертикальным (Ib)
потенциалами ионизации соотношением:
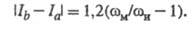
Разница величин (Ib
- Ia) м. б. использована в случае несложных 3- или 4-атомных
молекул для расчета изменений межатомного расстояния 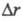 и валентного угла
и валентного угла 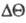 ,
обусловленных фотоионизацией:
,
обусловленных фотоионизацией:
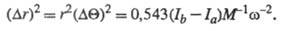
(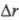 и r указаны в
и r указаны в 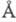 ,
M - в атомных единицах массы,
,
M - в атомных единицах массы, 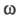 - в 1000 см-1).
- в 1000 см-1).
Измерения энергий связи
валентных электронов молекул в газовой фазе позволяет проверить точность теоретич.
расчетов, установить закономерности электронного строения молекул в изоэлектронных,
изовалентных и т. п. рядах, выявить влияние заместителей, установить их донорно-акцепторные
св-ва. Фотоэлектронные спектры известны примерно для 10000 своб. молекул.
Для твердых тел фотоэлектронная спектроскопия позволяет
определить положение уровня Ферми и распределение электронной плотности. При
изучении адсорбции м. б. установлены: характер присоединения молекулы к пов-сти
(физ. адсорбция или хемосорбция), природа взаимод. молекулы с пов-стью, роль
в этом взаимод. разл. мол. орбиталей. Важная характеристика - угловая зависимость
фотоэлектронного спектра, т. е. изменение интенсивности полосы при изменении
угла 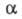 между направлением фотонов и нормалью к пов-сти, а также угла
между направлением фотонов и нормалью к пов-сти, а также угла 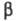 между нормалью к пов-сти и направлением вылета фотоэлектронов. Установлено,
напр., что молекула СО присоединяется по граням (111) кристаллов Pt и Pd таким
образом, что ось СО располагается вертикально, а при адсорбции по грани Pt (110)
ось СО отклонена от нормали к пов-сти на угол 26°.
между нормалью к пов-сти и направлением вылета фотоэлектронов. Установлено,
напр., что молекула СО присоединяется по граням (111) кристаллов Pt и Pd таким
образом, что ось СО располагается вертикально, а при адсорбции по грани Pt (110)
ось СО отклонена от нормали к пов-сти на угол 26°.
Относит. интенсивности
полос фотоэлектронных спектров позволяют качественно судить о составе атомных
орбиталей, линейная комбинация к-рых образует данную мол. орбиталь (см. ЛКАО-приближение).
Интенсивность полосы Iмо, связанной с нек-рой мол. орбиталью,
определяется интенсивностя-ми полос 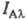 ,
связанных с атомными орбиталями
,
связанных с атомными орбиталями 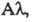 и заселенностями этих орбиталей
и заселенностями этих орбиталей 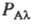 (по
Малликену):
(по
Малликену):
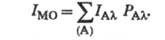
Интенсивности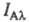 зависят
от энергии фотона hn, поэтому по изменению Iмо можно
качественно судить об участии разл.
зависят
от энергии фотона hn, поэтому по изменению Iмо можно
качественно судить об участии разл.
Al в образовании данной
мол. орбитали. Напр., для 3d-орби-тали Ni интенсивность полосы 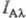 возрастает более чем в 10 раз при переходе от излучения He(I) к излучению Не(П),
поэтому рост интенсивности полосы для изучаемого электронного уровня молекулы
указывает на значит, вклад 3d-op-биталей в волновую ф-цию данного состояния.
возрастает более чем в 10 раз при переходе от излучения He(I) к излучению Не(П),
поэтому рост интенсивности полосы для изучаемого электронного уровня молекулы
указывает на значит, вклад 3d-op-биталей в волновую ф-цию данного состояния.
Лит.: Нефедов В.И.,
В о в н а В.И., Электронная структура химических соединений, M., 1987; их же,
Электронная структура органических и элементоорганических соединений, M., 1989;
Вовна В.И., Электронная структура органических соединений по данным фотоэлектронной
спектроскопии, M., 1991. В. И. Нефедов.