Аланин
АЛАНИН, мол. м. 89,09.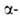 Аланин (
Аланин (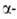 аминопропионовая к-та, Ala), A)CH3CH(NH2)COOH-кристаллы; т.пл. D, L-аланина 295-296 °С, L-аланина- 315-316 °С, D-аланина- 291 -293 °С (плавятся с разл.); для L-аланина
аминопропионовая к-та, Ala), A)CH3CH(NH2)COOH-кристаллы; т.пл. D, L-аланина 295-296 °С, L-аланина- 315-316 °С, D-аланина- 291 -293 °С (плавятся с разл.); для L-аланина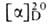 14,2° (концентрация 10 г в 100 мл 6 н. НС1); раств. в воде, плохо-в этаноле, не раств. в эфире. Для L-аланина рХа СООН и NH2 соотв. 2,34 и 9,6, рI-6,0.
14,2° (концентрация 10 г в 100 мл 6 н. НС1); раств. в воде, плохо-в этаноле, не раств. в эфире. Для L-аланина рХа СООН и NH2 соотв. 2,34 и 9,6, рI-6,0.
По хим. св-вам аланин-типичная алифатич.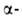 аминокислота. L-аланин-кодируемая аминокислота, встречается во всех организмах в своб. виде и в составе белков. D-аланин обнаружен только в бактериях и в опиоидных пептидах, выделенных из кожи южноамериканских лягушек. Биосинтез L-аланина происходит в результате аминирования и переаминирования пировиноградной к-ты или
аминокислота. L-аланин-кодируемая аминокислота, встречается во всех организмах в своб. виде и в составе белков. D-аланин обнаружен только в бактериях и в опиоидных пептидах, выделенных из кожи южноамериканских лягушек. Биосинтез L-аланина происходит в результате аминирования и переаминирования пировиноградной к-ты или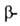 цекарбоксилирования аспара-гиновой к-ты.
цекарбоксилирования аспара-гиновой к-ты.
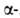 Аланин получают аммонолизом
Аланин получают аммонолизом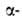 хлор(бром)пропионовой к-ты. В спектре ЯМР
хлор(бром)пропионовой к-ты. В спектре ЯМР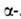 аланина величины хим. сдвигов (в м. д.) в D2O для протонов группы СН-3,778, СН3-1,481. L-аланин применяют для синтеза пептидов, в смеси с др. аминокислотами-для парэнтерального питания.
аланина величины хим. сдвигов (в м. д.) в D2O для протонов группы СН-3,778, СН3-1,481. L-аланин применяют для синтеза пептидов, в смеси с др. аминокислотами-для парэнтерального питания.
Впервые выделен из фиброина шелка в 1888, синтезирован А. Штреккером в 1850 омылением нитрила аланина, полученного взаимод. аммиаката ацетальдегида с HCN и НС1. Мировое произ-во L-аланина ок. 130 т/год (1982).
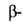 Аланин
Аланин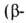 аминопропионовая к-та) Н2NСН2СН2СООН -кристаллы; т.пл. 200°С; раств. в воде, плохо-в спирте; рКа СООН и NН2 соотв. 3,6 и 10,19, рI-6,9. Структурный фрагмент кофермента А, пантотено-вой к-ты, ансерина и карнозина. Биосинтез:
аминопропионовая к-та) Н2NСН2СН2СООН -кристаллы; т.пл. 200°С; раств. в воде, плохо-в спирте; рКа СООН и NН2 соотв. 3,6 и 10,19, рI-6,9. Структурный фрагмент кофермента А, пантотено-вой к-ты, ансерина и карнозина. Биосинтез: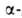 декарбоксилирование аспарагиновой к-ты или расщепление пиримидиновых оснований через дигидроурацил. Получают
декарбоксилирование аспарагиновой к-ты или расщепление пиримидиновых оснований через дигидроурацил. Получают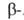 аланин действием избытка NH3 на акрилонитрил, акролеин или акриловую к-ту; взаимод. гипобромита щелочного металла с сукцинимидом. Применяют для приготовления буферных р-ров, синтеза пантотеновой к-ты и аналогов биологически активных пептидов. В. В. Баев.
аланин действием избытка NH3 на акрилонитрил, акролеин или акриловую к-ту; взаимод. гипобромита щелочного металла с сукцинимидом. Применяют для приготовления буферных р-ров, синтеза пантотеновой к-ты и аналогов биологически активных пептидов. В. В. Баев.
