БРОМАТОМЕТРИЯ, титриметрич. метод определения восстановителей,
а также орг. соед., вступающих с бромом в р-ции присоединения или замещения.
Основана на применении солянокислого р-ра КВrО3 с известным
титром. При титровании восстановителей бромат превращается в бромид по
схеме: BrO3- + 6Н+ + 6е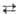 Вr-
+ ЗН2О (стандартный электродный потенциал + 1,45 В). Для ускорения
процесса анализируемые р-ры иногда нагревают до 40-70°С или добавляют к
ним катализаторы, напр. соли Hg(II), Mn(II). Конечную точку титрования
устанавливают с помощью окислит.-восстановит. индикаторов (метилового оранжевого,
метилового красного,
Вr-
+ ЗН2О (стандартный электродный потенциал + 1,45 В). Для ускорения
процесса анализируемые р-ры иногда нагревают до 40-70°С или добавляют к
ним катализаторы, напр. соли Hg(II), Mn(II). Конечную точку титрования
устанавливают с помощью окислит.-восстановит. индикаторов (метилового оранжевого,
метилового красного,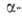 нафтофлавона,
хинолинового желтого и др.), по появлению желтой окраски брома, образующегося
при взаимод. избытка ВrО3- с Вr-, а также
потенциометрически или фотометрически. Метод применяют для определения
восстановителей - As(III), Sb(III), 71(1), Sn(II), Cu(I), Fe(II), H2O2,
гидразина, гидроксиламина, тиомочевины, аскорбиновой и щавелевой к-т и
др.
нафтофлавона,
хинолинового желтого и др.), по появлению желтой окраски брома, образующегося
при взаимод. избытка ВrО3- с Вr-, а также
потенциометрически или фотометрически. Метод применяют для определения
восстановителей - As(III), Sb(III), 71(1), Sn(II), Cu(I), Fe(II), H2O2,
гидразина, гидроксиламина, тиомочевины, аскорбиновой и щавелевой к-т и
др.
Нитрование орг. соед. ведут при избытке КВr, к-рый предварительно добавляют
в р-р титранта (бромид-броматная смесь) или в анализируемый р-р. При этом
с определяемым в-вом взаимод. бром, образующийся из ВrO3-
и Вг~ по ур-нию: BrOJ + 5Вr- + 6Н+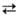 ЗВr2
+ ЗН2О. Поэтому этот вариант броматометрии (наз. также бромид-броматометрией)
иногда относят к бромометрии, т.е. к методу, основанному на применении
стандартного р-ра Вг2.
ЗВr2
+ ЗН2О. Поэтому этот вариант броматометрии (наз. также бромид-броматометрией)
иногда относят к бромометрии, т.е. к методу, основанному на применении
стандартного р-ра Вг2.
Если орг. в-во медленно взаимод. с выделяющимся Вr2, к анализируемому
р-ру прибавляют избыток бромид-броматной смеси и подкисляют; после завершения
бромироваия избыток Вr2 оттитровывают р-ром Na2S2O3
в присут. KI и крахмала в кач-ве индикатора или определяют обратным арсенитометрич.
методом. Последний основан на окислении AsO2- по
схеме: AsO2- + ЗН2О — 2е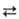 AsO43-
+ 4H+ (стандартный электродный потенциал — 0,56 В). В
этом случае к анализируемому р-ру, содержащему своб. бром, добавляют стандартный
р-р NaAsO2, избыток к-рого оттитровывают броматом в присут.
метилового оранжевого или метилового красного. Иногда для определения избытка
брома к р-ру добавляют избыток KI и оттитровывают выделившийся иод р-ром
Na2S2O3.
AsO43-
+ 4H+ (стандартный электродный потенциал — 0,56 В). В
этом случае к анализируемому р-ру, содержащему своб. бром, добавляют стандартный
р-р NaAsO2, избыток к-рого оттитровывают броматом в присут.
метилового оранжевого или метилового красного. Иногда для определения избытка
брома к р-ру добавляют избыток KI и оттитровывают выделившийся иод р-ром
Na2S2O3.
Бромид-броматометрию применяют для определения фенола, крезола, анилина,
резорцина, салициловой к-ты, 8-гидроксихинолина, ненасыщенных соед. (см.
также Бромное число), а также для косвенного определения катионов
Al, Mg, Mn(II), Ca, Ni, Co, Cu(II), Cd, Fe(III), La(III) и др., образующих
с 8-гидроксихинолином нерастворимые в воде комплексные соед., к-рые отделяют,
растворяют в к-те и оттитровывают выделившийся 8-гидроксихинолин. Т.М.
Малютина.
===
Исп. литература для статьи «БРОМАТОМЕТРИЯ»: нет данных
Страница «БРОМАТОМЕТРИЯ» подготовлена по материалам химической энциклопедии.