Тиоэфиры и дитиоэфиры; сульфиды и дисульфиды; органические сульфиды
Встречаются как примеси в неочищенной нефти; диаллилсульфид — в воздухе канализационных труб и колодцев.
Получаются: тиоэфиры — алкилированием неорганических сульфидов алкилгалогенидами или алкилсульфатами, алкилированием меркаптидов, термическим разло-
M = 213,53
Μ = 282,42
жением меркаптидов тяжелых металлов, взаимодействием меркаптанов с олефинами и окисями алкиленов; дитиоэфиры — при окислении меркаптанов.
Применяются как антиокислительные и стабилизирующие добавки к моторным топливам, смазочным маслам, латексам; как лекарственные препараты, красители, детергенты, растворители.
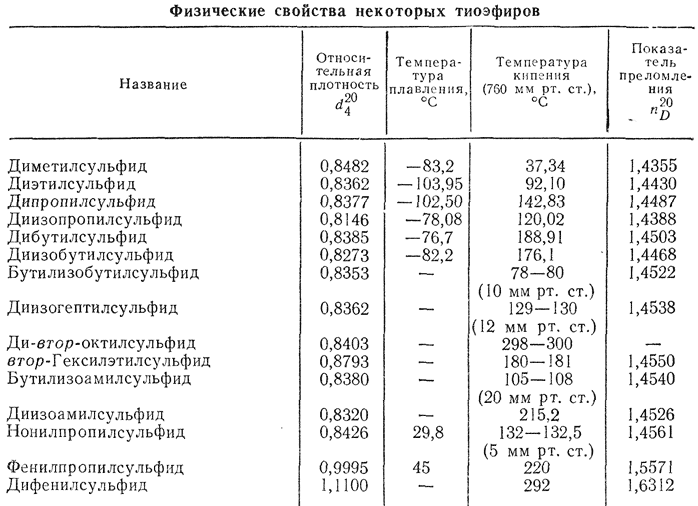
Физические свойства. Низшие алифатические тиоэфиры — бесцветные жидкости со слабым эфирным запахом, нерастворимые в воде, растворимые в органических растворителях. Температуры кипения выше, чем у соответствующих тиоспиртов. Ощущается неприятный запах: диметилсульфида при 0,07 мкг/л, диэтилсульфида при 0,01 мкг/л, диизоамилсульфида при 0,022 мкг/л, диаллилсульфида при 0,00065 мкг/л. Совершенно чистые тиоэфиры заметно не пахнут. См. также таблицу.
Химические свойства. Нейтральные вещества. Характерна способность окисляться в соединения с серой высшей валентности. Галогены присоединяются к тиоэфирам, образуя кристаллические продукты. При окислении тиоэфиров образуются вначале сульфоксиды (четырехвалентная сера), затем сульфоны (шестивалентная сера). Дитиоэфиры легко восстанавливаются до тиоспиртов.
Общий характер действия сходен с действием тиоспиртов. Возбуждают, а затем угнетают центральную нервную систему, вызывая глубокий наркоз при соответствующих концентрациях, а также дистрофические изменения во внутренних органах. Обладают хроноконцентрационным и раздражающим действием. Введение галогена увеличивает раздражающий и токсический эффект. На токсические свойства сильно влияет положение атомов галогена по отношению к сере. Более ядовиты тиоэфиры с ненасыщенными радикалами.


