Принса реакция
ПРИНСА РЕАКЦИЯ (Кривица-Принса р-ция), присоединение формальдегида к олефинам. В зависимости от условий, в к-рых осуществляют р-цию, образуются разл. конечные продукты. В присут. кислых катализаторов (H2SO4, Н3РО4, BF3, ZnCl2, SnCl4) в водной среде образуются 1,3-гликоли и 1,3-диоксаны (соотв. р-ции 1 и 2), в присут. НС1 или СН3СООН-соотв. хлоргидрины или ацетаты 1,3-гликолей, в безводной среде в присут. к-т Льюиса, а также в отсутствие катализаторов, но при высоких т-рах (ок. 200 °С)-непредельные спирты (в результате аллильной перегруппировки; р-ция 3):
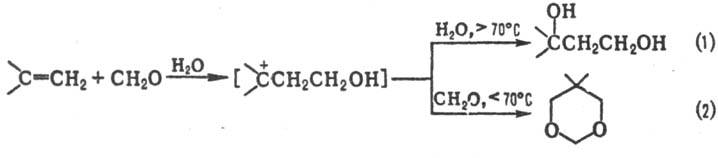
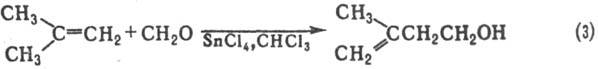
В условиях Принса реакции непредельные спирты и 1,3-гликоли могут превращ. в 1,3-диены, напр.:
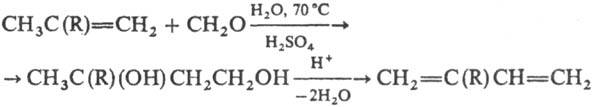
Наиб. легко в р-цию вступают несимметричные олефины и диены. Вместо формальдегида можно использовать ди-метилацеталъ, хлорметилалкиловые эфиры, перфторкетоны или хлораль. При использовании газообразных олефинов процесс обычно ведут под давлением. Выходы конечных продуктов обычно 20-50%.
Принса реакция часто сопровождается образованием изомерных продуктов (вследствие миграции алкильных групп в промежут. карбкатионе по такому же механизму, как в Вагнера -Меер-вейна перегруппировке). Нередко в качестве побочных в-в образуются также олигомеры и полимеры. Алкенилгалоге-ниды в условиях Принса реакции образуют преим. р-гидроксикислоты, напр.:
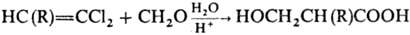
Механизм Принса реакции относительно хорошо изучен. Считается, что в присут. к-т формальдегид протонируется с образованием катиона ф-лы I. Последний присоединяется к олефи-ну, образуя карбкатион II, к-рый стабилизируется путем отщепления протона через циклич. переходное состояние:
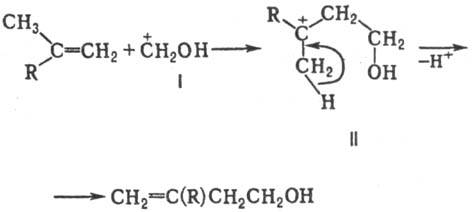
В присут. к-т Льюиса образуется промежут. соединение III, стабилизирующееся в результате отщепления к-ты Льюиса и переноса протона, напр.:
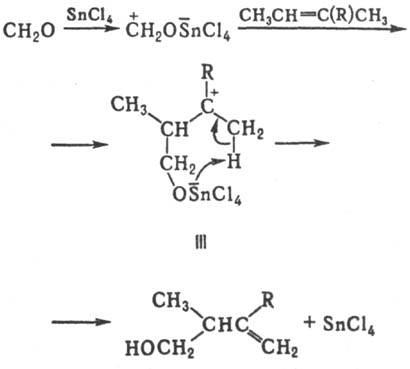
Установлено, что Принса реакция протекает как анти-присоединение. Одна из модификаций Принса реакции - циклизация ненасыщ. кетонов под действием кислых катализаторов (т. наз. циклореак-ция Принса), напр.:
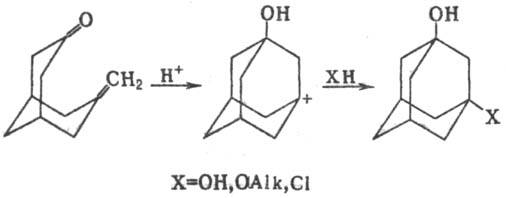
В пром-сти Принса реакцию используют для синтеза 1,3-гликолей, а также как одну из стадий для получения изопрена, в лаб. практике-для получения непредельных спиртов и 1,3-диоксанов.
Конденсация формальдегида с олефинами впервые осуществлена в 1899 О. Кривицем, в 1917 эта р-ция подробно изучена X. Принсом.
Лит.: Исагулянц В. И. [и. др.], "Успехи химии", 1968, т. 37, в. 1, с. 61-77; Wilkins С., Marianelli R., "Tetrahedron", 1970, v. 26, p. 4131-39; Griengl H.,Mayer A., Geppert K.. P., "Monatsh. Chem.", 1981, Bd 112, № 8-9, S. 1007-16. Г.И. Дрозд.
