Оливомицины
ОЛИВОМИЦИНЫ (антибиотики NSCA-649), О-гликозид-ные антибиотики, агликон к-рых представляет собой оливин, а гликозидная цепь-разл. комбинации 2,6-дидезокси-альдогексоз, образующие две неразветвленные ди- и три-сахаридные цепи (см. ф-лы I-IV). Открыты в 1962 Г. Граузе с сотрудниками как метаболиты Actinomyces olivoreticuli. С помощью адсорбц. хроматографии на силикагеле выделены 4 компонента: оливомицин А (ф-ла I), оливомицин В (И), оливомицин С (III) и оливомицин D (IV) (перечислены в порядке уменьшения подвижности) в соотношении 30:4:1:1 по массе.
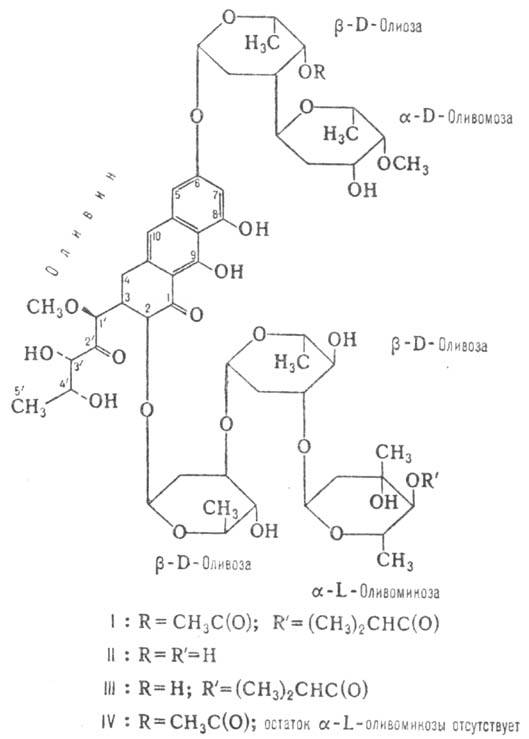
Содержащийся в наиб. кол-ве оливомицин А-желтые кристаллы с т. пл. 160-165°С, раств. в спиртах, хлороформе, диэтило-вом эфире, плохо-в воде, не раств. в ССl4, ароматич. и алифатич. углеводородах; [a]23D —35° (в этаноле); рКа 7,2. В спектрах поглощения р-ров оливомицина А в этаноле наблюдаются максимумы при 227, 277, 318, 333 и 406 нм (lg e 4,33, 4,71, 3,78, 3,68 и 4,16 соотв.); в ИК спектрах характеристич. полосы-1060, 1510, 1582, 1640, 1738 и 3880см-1. Синтезирован гептаацетат оливомицина А с т. пл. 212-214°С, 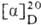 -22° (в СНС13). Оливомицин А образует комплексные соед. с металлами в степенях окисления >1, а также с борной к-той. Св-ва остальных оливомицинов аналогичны.
-22° (в СНС13). Оливомицин А образует комплексные соед. с металлами в степенях окисления >1, а также с борной к-той. Св-ва остальных оливомицинов аналогичны.
При подкислении р-ра оливомицин А последовательно отщепляет моносахаридные остатки с образованием серии гликози-дов - продуктов частичного гидролиза, один из к-рых - оливомицин D. Спектральные характеристики и кислотные св-ва всех оливомицинах определяются оливином. Последний образует 3',4'-ацетонид, при обработке щелочами превращ. в 3'-гидрокси-4'-оксо-изомер (изооливин), а при действии разл. окислителей расщепляется с образованием ацетальдегида и муравьиной к-ты, производных D-трео-2,3-дигидроксимасляной или D-винной к-ты.
Оливомицины и родственные им антибиотики активны против грам-положит. бактерий, причем активность снижается по мере последоват. отщепления моносахаридных остатков. Наиб. интерес представляет выраженная противоопухолевая активность, благодаря к-рой оливомицины и их аналоги применяют в онкологии, гл. обр. при комбинир. химиотерапии. В основе механизма их действия лежит ингибирование ДНК-зависимого синтеза РНК. Они тормозят процесс транскрипции, препятствуя движению ДНК-полимеразы вдоль днк.
Лит.: Remers W. A., The chemistry of antitumor antibiotics, v. 1, N.Y.-[a.o.], 1979, p. 133-75. Ю.А. Берлин.
