Молекулярная биология полисахаридов
Огромные успехи исследований механизмов кодирования наследственной информации и биосинтеза белка, ферментативного катализа и регулирования активности ферменов, действия антибиотиков и гормонов, всей той области изучения живого, которую принято называть молекулярной биологией, приучили всех к мысли о том, что в структурах молекул жизни положение буквально каждого атома строго обусловлено и подчинено выполнению предназначенных для этих молекул биологических функций. Именно в этом смысле принято обычно говорить о специфичности биополимеров, прочно ассоциировавшейся в сознании исследователей с однозначным соответствием между структурой и выполняемой функцией. При таком «комплексе структурного детерминизма» трудно было освоиться с представлением о специфичности полисахаридов, для многих из которых характерна статистичность структур, микрогетерогенность и, нередко, хаотичность распределения моносахаридных остатков по цепи. И, тем не менее, накапливающийся материал по сложному и высоко специализированному функционированию углеводных полимеров в живых системах убеждает в том, что и в этой области возможен и необходим перевод функциональных свойств биополимеров на язык молекулярных структур, т.е применим основной принцип молекулярной биологии. Только оперировать при этом нередко приходится с иными уровнями специфической упорядоченности их структур. Носителем функциональной специфичности, если можно так выразиться, здесь оказывается не некоторая одна ковалентная структура, а определенный тип ковалентной структуры. И этот тип может быть не менее строго детерминирован, чем единичная структура. Поэтому возникает задача сформулировать те типовые (а не индивидуальные) характеристики популяции различных молекул, составляющих углеводный биополимер, которые ответственны за его биологические функции. Именно такой подход к молекулярной биологии полисахаридов помог получить первые реальные успехи в этой области. Они связаны в первую очередь с именем Д.А.Риса (Англия), на идеях и результатах исследований которого в основном построено наше дальнейшее изложение.
Характерное свойство многих классов полисахаридов есть способность к гелеобразованию в водных растворах. Именно с этим свойством связан ряд биологических функций полисахаридов (а также ряд областей практического применения самих полисахаридов и их производных). Сюда, в первую очередь, относится обеспечение нужного набора механических свойств опорных систем (таких, например, как клеточные стенки), склеивающих и пластических свойств межклеточного вещества, упругости ряда систем (хрусталик глаза), функционирования смазочных материалов в живых организмах (синовиальная жидкость в суставах), материала поверхности эпителиальных клеток, вдоль которых движутся биологические жидкости (кровь, лимфа и т.п.), и других физико-механических и физико-химических характеристик строительных материалов живых систем. Очень наглядно роль гелеобразующей способности полисахаридов в обеспечении важных биологических функций можно проследить на следующем примере.
Водоросли прибрежных зон океана обитают в весьма своеобразных условиях: они подвергаются значительным волновым нагрузкам, направление и величина которых меняется по всем трем координатам в зависимости от ветров и микрорельефа, а водоросли литорали подвержены, кроме того, периодическим обсыханиям во время отливов. Чтобы противостоять таким воздействиям, красные и бурые водоросли выработали чисто «полисахаридное» приспособление. Все они содержа в качестве межклеточного вещества специфические кислые полисахариды (альгиновые кислоты в бурых водорослях и сульфатированные галактаны в красных), способные даже в разбавленных растворах образовывать прочные упругие гели, удерживающие значительные количества воды в «псевдотвердом» состоянии.
Именно упругий гель оказался той механической основой, которая идеально приспособлена к сопротивлению неподвижных организмов волнам, и одновременно великолепным аккумулятором воды, позволяющим водорослям литорали благополучно переживать отливы. Не случайно, именно бурые и красные водоросли служат важным источником гелеобразователей, применяемых в промышленности. Гелеобразующая способность относится к тем немногим функциональным свойствам углеводных биополимеров, которые в настоящее время удается трактовать на молекулярном уровне.
Для образования полисахаридного геля нужно, чтобы цепные молекулы были организованы в рыхлую пространственную сетку, в ячейках которой находится растворитель (вода). Одним из ключевых вопросов, ответ на который позволяет связать структуру полимера с его способностью к гелеобразованию, является природа узлов этой сетки. Это могут быть ковалентные связи между цепями, и в таком случае сетка представляет собой одну гигантскую трехмерную молекулу. Так построен, например, гликопептид бактериальной стенки, который мы уже рассмотрели, а из искусственных образований – сефадекс, полусинтетический материал для гель-хроматографии. Более типичны полисахаридные гели, в которых связи цепей в узлах не ковалентны.
Характерный пример кислых гелеобразующих полисахаридов представляют каррагинаны, содержащиеся в ряде красных водорослей. Эти полисахариды относятся к тому же типу альтернирующих структур, что и агароза, и могут быть обобщенно представлены формулой 11. Характерной и постоянной особенностью такой структуры является правильное чередование β -1 à 4 и α -1 à 3-связей, но при этом структура остатков А и В варьирует в определенных пределах. Остатки А в большинстве случаев представлены 3,6-ангидро- α -D-галактопиранозой (12) или ее 2-О-сульфатом (13), но могут быть и α -D-галактопираноза-6-сульфатом (14) и α -D-галактопираноза-2,6-дисульфатом (15). Остаток В – это β -D-галактопираноза (16), ее 2-О-сульфат (17) и 4-О-сульфат (18).
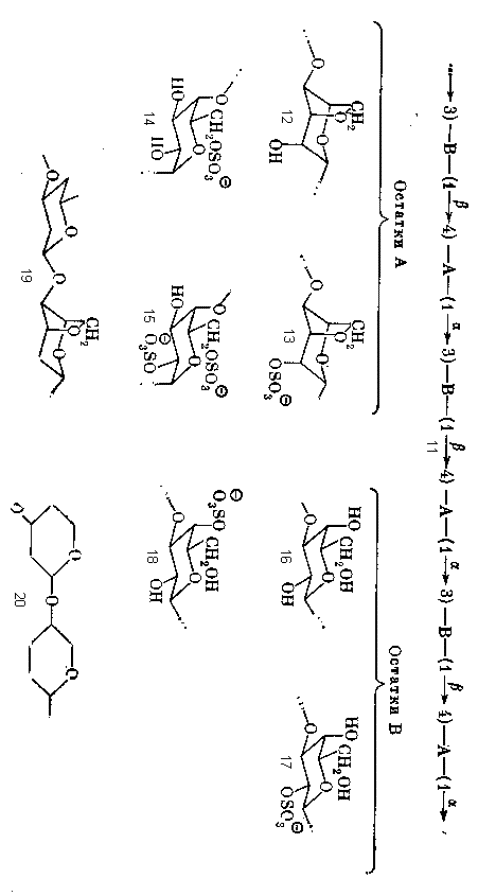
Если отвлечься от вариаций заместителей в пиранозных циклах и рассматривать только структуры с участием 3,6-ангидро-остатков, то повторяющееся звено таких цепей (-В-А-) можно представить формулой 19. Конформационно такое звено представляет собой отрезок стержня, одна из связей которого лежит на его продолжении, а другая отходит под некоторым углом к его оси, как видно на схематической проекции 20. Такое расположение связей создает предпосылки для спирализации цепи. Действительно, в опытах со специальным образом приготовленными образцами каррагинанов, структура которых достаточно приближается к регулярной с повторяющимся звеном типа 19, при помощи рентгеноструктурного анализа было показано существование спиральной конформации цепей.
Интересно и важно для дальнейшего, что спираль оказалась двойной: две цепи с одинаковым направлением гликозидных связей тесно связаны водородными связями и закручены в главную спираль с шагом 26 Å . Такая двойная спираль является довольно устойчивым образованием. Геометрические параметры каждой отдельной цепи диктуются конформацией повторяющегося звена 19 и хорошо обосновываются теоретическими методами современного конформационного анализа полимеров. Шаг этой спирали достаточно велик, так что между соседними витками остается большой промежуток («пружина» сильно растянута). В этот промежуток точно укладываются витки второй спирали; причем таким образом, что между соседними остатками из двух разных цепей возникают водородные связи, поддерживающие стабильность всей конструкции.
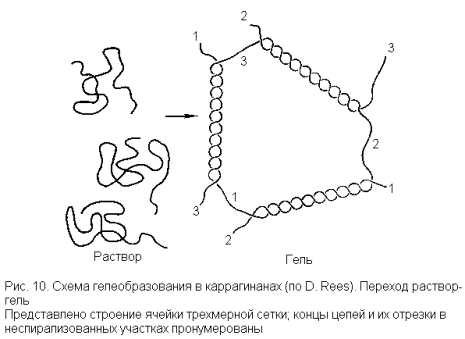
В свете этих данных образование трехмерной сетки из линейных молекул каррагинана, обусловливающей гелеобразование, трактуется следующим образом. В сильно разбавленном растворе (или при достаточно высокой температуре), когда межмолекулярные взаимодействия малы, форма цепей аппроксимируется конформацией беспорядочного клубка. В более концентрированных растворах (или при охлаждении) начинается образование двойных спиралей, связывающих участки разных молекул. Некоторая произвольно выбранная (и достаточно длинная) молекула может при этом образовывать несколько таких участков связывания и не с одной, а с несколькими молекулами. Тогда возникают нековалентные поперечные сшивки, и создается трехмерная сетка (рис. 10).
Теперь можно рассмотреть требования к ковалентной структуре полисахаридной цепи (в рамках общей структуры 11), соблюдение которых необходимо для возникновения такой пространственной сетки. Первым условием является возможность спирализации, для чего необходимы участки цепей из повторяющихся звеньев типа 19. Эти участки должны быть регулярными в смысле правильного чередования таких звеньев, но могут быть нерегулярными по положению и распределению сульфата. В то же время вся цепь или ее значительная часть не должна иметь регулярную структуру из повторяющихся звеньев типа 19.
Действительно, в таком случае спирализация приводила бы к ассоциированию каждой молекулы только с одной другой молекулой (образовывалась бы непрерывная двойная спираль) и сетка не могла бы образовываться. Макроскопически это привело бы лишь к повышению кажущейся молекулярной массы полисахарида или к дальнейшей ассоциации с выпадением осадка, но не к гелеобразованию. В то же время регулярные участки не должны быть слишком короткими, так как в этом случае двуспиральные связки (узлы сетки) оказались бы чересчур слабыми или не образовывались бы совсем.
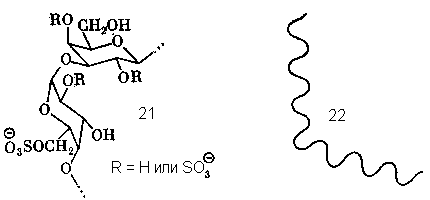
Следовательно, в структуре гелеобразующего полисахарида должны быть и регулярные последовательности типа 19, и нарушения регулярности, места, где конформация цепи резко меняется. Такую роль играют варианты звеньев типа А – сульфаты 14 и 15. Действительно, конформация дисахаридного блока –А-В- с участием (21) резко отличается от таковой для блока с 3,6-ангидрозвеном (19). Поэтому в тех точках цепи, где звено типа 12 или 13 заменено на сульфатированное звено типа 14 или 15, правильная спираль претерпевает излом (22) и связка цепей в виде двойной спирали в этом месте нарушается. Отсюда видно, что отклонения от регулярности, дефекты правильной структуры, суть не ошибки биосинтеза, как может показаться на первый взгляд, а биологически осмысленный, функционально необходимый элемент структуры.
Прочность геля и содержание в нем воды (зависящее от средних размеров ячеек) определяется в основном двумя параметрами: длиной спирализуемых и длиной неспирализуемых участков, т.е. распределением различных остатков вдоль цепи. Здесь уместно заметить, что «деспирализующие» остатки 14 и 15 являются биохимическими предшественниками 3,6-ангидрозвеньев 12 и 13. Дело в том, что биосинтез полисахаридов типа каррагинанов включает, по-видимому, сульфатирование регулярной незамещенной цепи типа …-A-B-A-B-A-B-… и замыкание ангидрозвеньев по схеме:
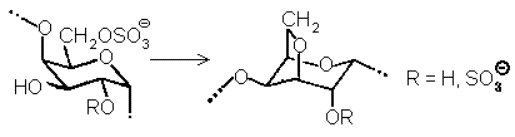
Таким образом, последняя стадия, осуществляемая уже на готовом полисахариде, создает гелеобразующую структуру, а степень ее протекания определяет физико-химические свойства геля. Можно полагать, что, управляя такой циклизацией, водоросли способны к тонкой адаптации своих механических характеристик к конкретным условиям среды. Например, продуцируя или активируя дополнительные количества фермента, катализирующего образование ангидроциклов, организм добивается быстрого повышения степени спирализации и, следовательно, адаптационного изменения свойств геля.
На примере каррагинанов можно проследить своеобразный характер специфичности структур таких полисахаридов. Очевидно, в этом случае не имеет большого функционального значения точная последовательность всех мономерных остатков в цепи; однако необходимым является чередование участков цепей, регулярных по альтернированию остатков β -D-галактопиранозы и 3,6-ангидро- α -D-галактопиранозы со связями 1 à 3 и 1 à 4, и участков с нарушениями такой регулярности – заменами ангидрозвеньев на соответствующие сульфаты типа 14 и 15.
Далее, функционально важно, чтобы эти участки имели определенную длину (не слишком большую и не слишком малую), но эта длина может варьировать в некоторых пределах без заметного влияния на функциональные свойства. В деспирализованных участках остатки типа 12 или 13, с одной стороны, и остатки типа 14 и 15, с другой, в известных пределах кажутся взаимозаменяемыми без заметных изменений свойств полисахарида, тогда как в спирализованных участках замена даже одного 3,6-ангидро-звена на его предшественник (сульфат 14 или 15) должна драматически сказаться на гелеобразующей способности полисахарида.
Как видно уже из структуры остатков типа А и В (12-18), число и положение сульфатных групп может варьировать в довольно широких пределах, но явно недопустимым представляется, например, наличие в остатках типа А сульфогруппы в положении 3 или ее отсутствие в положение 6 на стадии биосинтеза, предшествующей циклизации, так как из таких остатков не могли бы образовываться ангидрозвенья.
Конфигурация всех асимметрических центров в моносахаридных остатках каррагинанов строго детерминирована, однако, как показывает строение этих полисахаридов с близкородственными по структуре и свойствам сульфатированными полисахаридами типа агара (например, с агарозой и порфираном), в остатках типа А удивительным образом оказывается возможным обращение конфигурации всех ассиметрических центров сразу: замена остатков 3,6-ангидро-D-галактозы на остатки 3,6-ангидро-L-галактозы без сущесвенного изменения функции этих полисахаридов в водорослях (такой случай «безнаказанной» взаимозаменяемости оптических антиподов, по-видимому, уникален во всей биоорганической химии). Таким образом, видно что понятие специфичности полисахаридов, по крайней мере, для разобранного примера, следует относить к типу структуры, а не к индивидуальным структурам.
В других гелеобразующих полисахаридных системах могут быть иные (и весьма разнообразные) механизмы связывания макромолекул в узлах сетки; однако характер требований к ковалентной струкуре, соблюдение которых обеспечивает выполнение обусловленных гелеобразованием функций, оказывается сходным. Так, например, в гелях альгинатов, т.е. солей альгиновой кислоты, построенной из 1 à 4-связанных остатков β -D-маннуроновой (23) и α -L-гулуроновой (24) кислот, узлы образованы кристаллитами – правильным образом упакованными участками разных молекул с регулярной структурой, подобными по упаковке кристаллическим участкам элементарных фибрилл целлюлозы. Как мы уже говорили, цепи альгиновых кислот построены по блочному принципу: в них чередуются сегменты регулярной структуры из остатков одного типа с сегментами, в которых остатки обоих типов распределены более или менее случайно. Регулярные участки, подобно целлюлозе, имеют стержнеобразную конформацию и потому способны ассоциировать в кристаллиты, а для нерегулярных участков правильная упаковка невозможна, и они образуют в сетке промежутки между узлами.

Сходный тип узлов (кристаллиты) образуется в гелях пектинов – сложных разветвленных полисахаридов, в основе молекул которых лежит цепь из β -1 à 4-связанных остатков частично этерифицированной D-галактуроновой кислоты.
Связи цепей в кристаллитах пектинов сравнительно слабы и легко разрываются за счет гидратации моносахаридных остатков. Поэтому прочные гели образуются только при условии снижения термодинамической активности растворителя (воды) за счет растворения хорошо гидратируемых низкомолекулярных веществ (например, сахарозы). Образование пектиновых гелей в присутствии сахарозы есть физико-химическая основа ряда кондитерских проиводств, таких, как изготовление варенья, конфитюров, мармеладов и т.п. В растительных же тканях пектиновые гели служат связующим межклеточным материалом и цементирующей основой клеточной стенки.
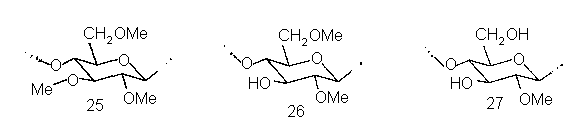
Еще один интересный гелеобразователь практического значения – частично метилированная целлюлоза, часто называемая «метилцеллюлозой». По мономерному составу это производное характеризуется случайным распределением метильных групп: в нем есть остатки и три-О-метил-глюкозы 25, и ди-О-метил-глюкоз (например, 26), и моно-О-метил-глюкоз (например, 27), и неметилированные остатки глюкозы. Онако по условиям получения частично метилированная целлюлоза характеризуется блочным строением. Дело в том, что ее синтез выполняют путем обработки нерастворимого целлюлозного материала хлористым метилом и водной щелочью. При этом происходит сильное набухание и затем интенсивное метилирование аморфных участков микрофибрилл, тогда как фрагменты молекул, находящиеся в кристаллических участках, почти недоступны для реагентов и остаются интактными. В результате в получающемся производном чередуются сегменты цепей, характеризующихся высокими степенями метилирования, с сегментами, не метилированными совсем (или очень незначительно метилированными).
В водных растворах высоко метилированные участки разных цепей связываются гидрофобными взаимодействиями и образуют узлы сетки, а низкометилированные и потому хорошо гидратированные участки образуют межузельные промежутки. Понятно, таким образом, что гелеобразующие свойства такого производного существенным образом зависят от тонкой структуры микрофибрилл и, следовательно, от происхождения исходного целлюлозного материала. Нам представляется, что пример метилцеллюлозы, хотя и не связан непосредственно с биологической функцией полисахаридов, весьма интересен: с одной стороны, это хорошая модель биологических гелей, а с другой – образец того, как чисто технические свойства материала непосредственно зависят от надмолекулярной структуры такого чисто биологического объекта, как клеточная стенка растения – источника сырья.
Нам хочется выразить уверенность, что и другие биологические функции углеводов в обозримом будущем можно будет перевести на строгий язык ковалентных структур; причем для разного типа функций можно ожидать весьма различную по характеру структурную специфичность, совсем не обязательно сводящуюся к типовой. И тогда огромное и несколько хаотическое многообразие углеводных структур перестанет восприниматься как странная игра природы, а органично войдет как составная часть в систему представлений молекулярной биологии.

