Глимы
ГЛИМЫ, диметиловые эфиры моно-, ди-, триэтиленгликолей и т.д. общей ф-лы СН3О(С2Н4О)nСН3, где п = 1,2,3 и т.д. Бесцв. жидкости (см. табл.); раств. в воде и орг. р-рителях, в т. ч. и в углеводородах.
Названия глимов производят, прибавляя к слову "глим" приставку, обозначающую исходный этиленгликоль, напр. моно-, ди- или триглим-соотв. диметиловые эфиры моно-, ди- или триэтиленгликоля.
СВОЙСТВА НЕКОТОРЫХ ГЛИМОВ

Ввиду прочности связи С—О глимы малореакционноспо-собны. Однако моноглим легко окисляется.
Получают глимы метилированием монометиловых эфиров этиленгликолей, напр. диметилсульфатом, или их алкоголятов метилгалогенидом. Наиб. значение имеет диглим. Его
производят в пром-сти нагреванием метанола,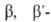 дихлордиэтилового эфира (хлорекса) в присут. щелочи при 60oС; диглим-сырец отделяют и подвергают ректификации. Глимы- инертные высококипящие р-рители.
дихлордиэтилового эфира (хлорекса) в присут. щелочи при 60oС; диглим-сырец отделяют и подвергают ректификации. Глимы- инертные высококипящие р-рители.
Т. всп. в открытом тигле 1 °С (моноглим), 67,2 oС (диглим) и 111oС (триглим). Б. Б. Чесноков.

Дополнения: