2-Метилфуран (Сильван)
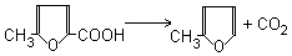
Предложили: А.Л.Мнджоян, Г.Т.Татевосян
Проверили: В.Г.Африкян, Г.Л.Папаян
Получение
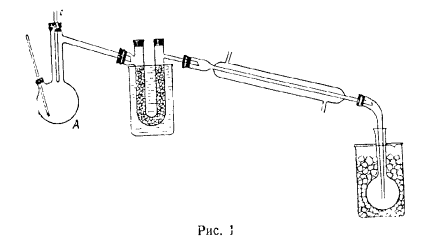
В перегонную колбу А (рисунок 1) емкостью 150 мл с тубусом для термометра, доходящего почти до дна колбы и с высоко расположенной широкой отводной трубкой, помещают 63 г (0,5 моль) 5-метилфуран-2-карбоновой кислоты с температурой плавления 108-109 градусов. Горло колбы закрывают пробкой, через которую проходит длинная стеклянная палочка Б, служащая для сбрасывания сублимирующейся исходной кислоты. Отводная трубка колбы А соединена с большой U-образной трубкой, заполненной кусками едкого натра, величиной с горошину и для предотвращения конденсации сильвана полностью погруженной в нагретую до кипения водяную баню, в качестве каковой удобно использовать высокий стакан емкостью 1 литр (примечание). Боковой отвод U-образной трубки соединен с наклонным холодильником, к которому присоединен длинный аллонж, конец аллонжа глубоко погружен в длинногорлую колбу емкостью 100 мл, служащую приемником и охлаждаемую ледяной водой.
При нагревании колбы исходная кислота сначала плавится, а затем начинает разлагаться. Температуру жидкости поддерживают при 170-175 градусов, при этой температуре происходит довольно быстрое декарбоксилирование и равномерная отгонка образующегося сильвана. Сублимирующуюся и осаждающуюся на горлышке колбы кислоту время от времени сбрасывают стеклянной палочкой обратно в колбу. К концу опыта остается незначительное количество жидкости, но на верхних частях стенок колбы образуется слой сублимировавшейся кислоты. Для разложения этого остатка температуру повышают до 230 градусов, прикрывая верхние части и горлышко колбы листами асбеста. Весь процесс длится 2,5-3 часа.
Собранный в приемнике влажный продукт переносят в делительную воронку, отделяют от незначительного количества перегнавшейся воды и высушивают сильван несколькими кусочками плавленного поташа. После второй перегонки получают 32,9-34,8 г или 80,1-84,8% теоретического количества чистого сильвана с температурой кипения 61 градус/680 мм.
Сильван, C5H6O, молярный вес 82,10, бесцветная, мало растворимая в воде, легко растворяющаяся в спирте и эфире жидкость с эфирным запахом; температура кипения 64-65 градусов/760 мм; d204 0,9159; nD20 1,4344. При стоянии на воздухе принимает светлую зеленовато-желтую окраску.
Примечания
U-образная трубка с едким натром служит для поглощения образующейся при декарбоксилировании углекислоты.
Едкий натр удерживает также значительную часть образующейся воды.
Другие способы получения
Сильван является отходом лесохимической промышленности; он образуется при сухой перегонке дерева и выделяется в больших количествах из головного погона древесной смолы1.
Синтетический сильван получается каталитическим гидрированием фурфурола в паровой фазе над медным2 и медно-хромовым3 катализаторами при температурах выше 200 градусов.
При пропускании фурфурилового спирта над окисью алюминия при 390 градусов4 или при нагревании его с никелевым катализатором при 150 градусах5 образуется смесь фурфурола, фурана и сильвана.
Описанный выше способ лабораторного получения сильвана основан на применении реакции термического декарбоксилирования 5-метилфуран-2-карбоновой кислоты6.
- см. например А.А. Прянишников, И.А.Григоров, Лесохимическая промышленность, №7, 12 (1939)
- Американский патент 2456187; C.A. 43,2218h (1949); Американский патент 2458001; C.A. 43m 2805h (1949); Британский патент 634079; C.A. 44,6886 (1950)
- L.E. Schiepp, H.H.Geller, K.W.Korff, J.Am.Chem.Soc. 69,672 (1947); K.Tsuda; Sh. Yoshida, M.Yanada, Y.Maruya, J.Pharm Soc. Japan 66,58 (1946); C.A. 45, 6182g (1951)
- R.PaulC.r. 200, 1118 (1935); Bullsoc. Chim. [5,] 2,2220 (1935)
- R. Paul, Bull. Soc. Chim. 8,507 (1940)
- H.Gilman, A.M.Janneym, C.W.Bradley, IowaStateCell. J. Sci. 7,429 (1933); C.A. 28,763 (1934); S.Machida, J.Chem.Soc. Japan 64,1311 (1943); C.A. 41,4182 (1947)