4.2.3. Определение константы диссоциации поверхностных ионных групп методом измерения электрокинетического потенциала
При наличии на поверхности одного типа групп, например, карбоксильных, допуская, что поверхностный потенциал определяется именно диссоциацией этих групп, и полагая, что поверхностный потенциал можно отождествлять с потенциалом в плоскости скольжения двойного ионного слоя, и, наконец, полагая, что концентрация может быть использована в расчетах вместо активностей, можно рассчитать константу диссоциации поверхностных групп по результатам измерения электрокинетического потенциала. Действительно, по предложению Оттевила константу равновесия диссоциации поверхностных групп можно выразить, как
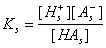 , (1.4.34)
, (1.4.34)
где 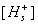 – равновесная концентрация ионов Н+ в плоскости скольжения;
– равновесная концентрация ионов Н+ в плоскости скольжения; 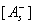 ,
,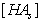 – концентрация ионизированных и неионизированных групп в поверхностном слое.
– концентрация ионизированных и неионизированных групп в поверхностном слое.
Предполагается, что распределение ионов Н+ можно описать уравнением Больцмана
 , (1.4.35)
, (1.4.35)
где [H+] - концентрация ионов водорода в объеме, F– число Фарадея.
Тогда
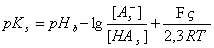 . (1.4.36)
. (1.4.36)
При достаточно высоких концентрациях электролитов величина z-потенциала невелика, и тогда можно ввести замену
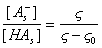 , (1.4.37)
, (1.4.37)
где z0 – потенциал при полной ионизации групп на поверхности, определяемый как максимальное значение, достигаемое зависимостью z = f(pH).
При z = z0/2 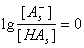 , тогда
, тогда
 . (1.4.38)
. (1.4.38)
Экспериментальные данные для разных карбоксилсодержащих и полистирольных диализованных латексов хорошо описываются единой зависимостью, которая при экстраполяции 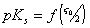 к z0 =0 дает величину pKs = 4,64, близкую к значению pK= 4,6, найденному методом титрования.
к z0 =0 дает величину pKs = 4,64, близкую к значению pK= 4,6, найденному методом титрования.


