Циановая и изоциановая кислоты
Для соединений радикалов циана —C≡N или изоциана C←=N— с гидроксилом возможны структурные формулы:

Кроме того, возможна еще и третья формула:
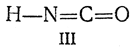
Соединение строения I называется циановой кислотой, а строения III — изоциановой кислотой. Структурная формула II приписывается гремучей кислоте.
Как видно из приведенных формул, циановая и изоциановая кислоты находятся в таутомерных отношениях. Как и в случае синильной кислоты, до настоящего времени известна лишь одна циановая кислота. Соли ее также существуют лишь в одной форме. В то же время сложные эфиры, т. е. продукты замещения в циановой кислоте водорода на углеводородные радикалы, известны в обеих изомерных формах

хотя первые и не были получены в чистом виде.
При окислении цианистого калия сплавлением с окисью свинца или при окислении безводного ферроцианида нагреванием с сухим бихроматом калия получается соединение KOCN, называемое циановокислым калием. Обменным разложением из калиевой соли можно получить труднорастворимую серебряную соль AgOCN, а также аммониевую соль NH4OCN, с помощью которой Вёлер осуществил первый синтез органического вещества — синтез мочевины:
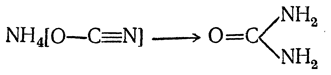
Вопрос о строении солей циановой кислоты не вполне ясен, так же как и в случае солей синильной кислоты. Реакции образования из них производных изоциановой кислоты (см. ниже) могут быть объяснены первоначальным присоединением алкилирующего реагента: