Бериллия фторид
БЕРИЛЛИЯ ФТОРИД BeF2, кристаллич. или аморфное в-во. До 220°С устойчива модификация с гексаген, решеткой типа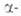 кварца (а = 0,4750 нм, с = 0,5186 нм, z = 3); плотн. 1,97 г/см3; С°р 51,84 Дж/(моль*К);
кварца (а = 0,4750 нм, с = 0,5186 нм, z = 3); плотн. 1,97 г/см3; С°р 51,84 Дж/(моль*К);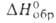 -1027 кДж/моль,
-1027 кДж/моль,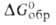 -979,9 кДж/моль; 5o298 53,3
-979,9 кДж/моль; 5o298 53,3
Дж/(молъ*К). Эта модификация при нагр. переходит в гексагональную типа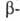 кварца с т. пл. 550°С и
кварца с т. пл. 550°С и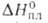 4,77 кДж/моль. Известна также тетрагон. модификация (типа
4,77 кДж/моль. Известна также тетрагон. модификация (типа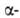 кристобалита), к-рая при 130°С переходит в кубическую типа
кристобалита), к-рая при 130°С переходит в кубическую типа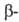 кристобалита с т. пл. 800°С. Т. кип. 1175СС,
кристобалита с т. пл. 800°С. Т. кип. 1175СС,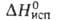 200 кДж/моль. Бериллия фторид гигроскопичен, раств. в воде (846 г/л при 25 °С), не раств. в этаноле. Гидролизуется р-рами щелочей и водой при нагревании, взаимод. с H2SO4. Получают BeF2 разложением (NH4)2BeF4 при 800-1100°С, значительно реже - взаимод. ВеО с газообразным HF. Магниетермич. восстановлением BeF2 получают металлич. Be. Бериллия фторид - компонент фторобериллатных стекол и солевой смеси ядерных реакторов на расплавл. солях. Бериллия фторид токсичен; ПДК 0,001 мг/м3.
200 кДж/моль. Бериллия фторид гигроскопичен, раств. в воде (846 г/л при 25 °С), не раств. в этаноле. Гидролизуется р-рами щелочей и водой при нагревании, взаимод. с H2SO4. Получают BeF2 разложением (NH4)2BeF4 при 800-1100°С, значительно реже - взаимод. ВеО с газообразным HF. Магниетермич. восстановлением BeF2 получают металлич. Be. Бериллия фторид - компонент фторобериллатных стекол и солевой смеси ядерных реакторов на расплавл. солях. Бериллия фторид токсичен; ПДК 0,001 мг/м3.
С фторидами щелочных металлов и аммония BeF2 образует фторобериллаты. Тетрафторобериллат аммония (NH4)2BeF4-кристаллы; при нагр. разлагается последовательно до NH4BeF3 и BeF2; C°p 211 Дж/(моль*К);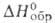 - 1990 кДж/моль,
- 1990 кДж/моль,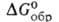 - 1728 кДж/моль; So298 250 Дж/(моль*К); раств. в йоде (32,2% по массе при 25°С) и р-рах NH4F. Получают: взаимод. ВеО с водными р-рами HF или NH4HF2 с послед, добавлением NH3 и выпариванием; р-цией ВеО или Ве(ОН)2 с безводным NH4HF2 при 100-200 °С.
- 1728 кДж/моль; So298 250 Дж/(моль*К); раств. в йоде (32,2% по массе при 25°С) и р-рах NH4F. Получают: взаимод. ВеО с водными р-рами HF или NH4HF2 с послед, добавлением NH3 и выпариванием; р-цией ВеО или Ве(ОН)2 с безводным NH4HF2 при 100-200 °С.
Тетрафторобеоиллат лития Li2BeF4 - кристаллы; т. пл. 459,1 °С;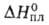 43,9 кДж/моль; С° 135 Дж/(моль*К);
43,9 кДж/моль; С° 135 Дж/(моль*К);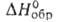 -2272 кДж/моль,
-2272 кДж/моль,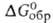 -2170 кДж/моль; So298 130 Дж/(моль*К); умеренно раств. в воде; растворяет UF4, ThF4, ZrF4 и др. фториды. Получают сплавлением BeF2 с LiF. Используют как компонент солевой смеси ядерных реакторов на расплавл. солях.
-2170 кДж/моль; So298 130 Дж/(моль*К); умеренно раств. в воде; растворяет UF4, ThF4, ZrF4 и др. фториды. Получают сплавлением BeF2 с LiF. Используют как компонент солевой смеси ядерных реакторов на расплавл. солях.
Тетрафторобериллат натрия Na2BeF4 - кристаллы; т. пл. ок. 590°С; раств. в воде (1,37% по массе при 20°С). Получают спеканием бериллиевых концентратов с Na2SiF6 и Na,CO3 при 750-800°С или сплавлением BeF2 с NaF; в лаб. - взаимод. Ве(ОН)2 с фтористоводородной к-той и Na2CO3. Промежут. продукт в произ-ве Ве(ОН)2 и др. соединений Be.
Лит. см. при ст. Бериллий. Э. Г. Раков.
