Циркония галогениды
ЦИРКОНИЯ ГАЛОГЕНИДЫ. Дигалогениды ZrX2 - черные кристаллы (табл.). Тригалогениды ZrX3 - голубовато-серые, темно-синие или черные кристаллы, к-рые могут существовать в сравнительно широких областях гомогенности, диспропорционируют или разлагаются при натр., легко окисляются на воздухе, не раств. в воде; получают их восстановлением соответствующих тетрагалогенидов. Тетрагалогениды ZrX4 -бесцв. кристаллы, гидролизуются водой (ZrF4 - медленно). Галогеноцирконаты(IV) - бесцв. кристаллы.
Тетрафторид ZrF4: 64,4 кДж/моль,
64,4 кДж/моль,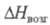 215,9 кДж/моль (1179 К); ур-ние температурной зависимости давления пара lgр (Па) = 15,6818 - 12430/Т (681-913 К); умеренно раств. в воде (15 г/л), лучше - в разб. к-тах; образует моно- и тригидрат, фтороциркониевые к-ты (фтороцирконаты гидроксония), напр. HZrF5 х nH2O, H2ZrF6 х nH2O, (H3O)2ZrF6, многочисленные фтороцирконаты, напр. NH4ZrF5, K2ZrF6, (NH4)3ZrF7, Ba2ZrF8, K2NiZr2F12, Na5Zr3F17. Получают из водных р-ров солей Zr(IV) действием фтористоводородной к-ты с послед. сушкой осадка в атмосфере HF, взаимод. ZrO2 с F2 или HF при 400-500 °С, термич. разложением (NH4)2ZrP6 или (NH4)3ZrF7 при 350-450 С. Применяют ZrF4 как промежут. в-во при металлотермич. произ-ве Zr, компонент фтороцирконатных стекол для волоконных световодов ИК диапазона, лазеров и хим. сенсоров.
215,9 кДж/моль (1179 К); ур-ние температурной зависимости давления пара lgр (Па) = 15,6818 - 12430/Т (681-913 К); умеренно раств. в воде (15 г/л), лучше - в разб. к-тах; образует моно- и тригидрат, фтороциркониевые к-ты (фтороцирконаты гидроксония), напр. HZrF5 х nH2O, H2ZrF6 х nH2O, (H3O)2ZrF6, многочисленные фтороцирконаты, напр. NH4ZrF5, K2ZrF6, (NH4)3ZrF7, Ba2ZrF8, K2NiZr2F12, Na5Zr3F17. Получают из водных р-ров солей Zr(IV) действием фтористоводородной к-ты с послед. сушкой осадка в атмосфере HF, взаимод. ZrO2 с F2 или HF при 400-500 °С, термич. разложением (NH4)2ZrP6 или (NH4)3ZrF7 при 350-450 С. Применяют ZrF4 как промежут. в-во при металлотермич. произ-ве Zr, компонент фтороцирконатных стекол для волоконных световодов ИК диапазона, лазеров и хим. сенсоров.
Гексафтороцирконат(IV) калия K2ZrF6 умеренно раств. в воде; получают осаждением из р-ров ZrF4 или (NH4)2ZrF6 действием солей К, в пром-сти - взаимод. рудных цирконовых концентратов с K2SiF6 при 600-700 °С; промежут. в-во для электролитич. произ-ва Zr. Гептафтороцирконат(IV) аммония (NH4)3ZrF7 разлагается при 300-400 °С с последоват. образованием (NH4)2ZrF6, NH4ZrF5 и ZrF4; хорошо раств. в воде; получают взаимод. ZrO2 с NF4HF2, при 150-200 °С; применяют для произ-ва особо чистого ZrF4 и получения др. фтороцирконатов. Оксифториды ZrOF2, Zr3OF10, Zr3O2F8, Zr4OF14, Zr2OF6, Zr7O9F10 и др.- бесцв. кристаллы; получают взаимод. ZrF4 с ZrO2, как промежут. продукты пирогидролиза ZrF4 или фторирования ZrO2.
ХАРАКТЕРИСТИКА ГАЛОГЕНИДОВ ЦИРКОНИЯ
| В-во | Сингония | Параметры кристаллической решетки | Т. пл.,°С | Т. кип.,0С | Плотн., г/см3 | 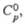 Дж/(моль х К) | 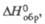 кДж/моль | 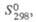 Дж/(моль х К) | ||||
| а, им | b, нм | с, нм | угол, град | |||||||||
| ZrF2 | Ромбич. | 0,409 | 0,491 | 0,656 | — | 902 | Разл. | — | 65,9 | — | 84 | |
| ZrF, | Кубич. | — | — | — | — | Разл. | — | 4,26 | 83,7 | — | 105 | |
| ZrF4 | Моноклинная | 0,957 | 0,993 | 0,773 | 94,47 | 690* | — | 4,55 | 103,6 | -1911 | 104 | |
| Тетрагон. | 0,7896 | — | 0,7724 | — | 910 | 906** | 4,61 | — | — | — | ||
| ZrF4 x H2O | Тетрагон. | 0,7724 | — | 1,1678 | — | Разл. | — | 3,53 | — | -2207 | — | |
| (H3O),ZrF6 | Моноклинная | 0,6715 | 0,7187 | 1,2626 | 11,83 | Разл. | — | — | — | — | — | |
| K2ZrF6 | Ромбич. | 0,661 | 0,141 | 0,697 | — | 240* | — | 3,58 | — | — | — | |
| K3ZrF7 | Кубич. | 0,899 | — | — | — | 920 | — | 3,12 | — | — | — | |
| (NH4)2ZrF6 | Ромбич. | — | — | — | — | 138* | Разл. | — | 234 | -2897 | 260 | |
| (NH4)3ZrF7 | Кубич. | 0,942 | — | — | — | Разл. | — | 2,21 | 300 | -3365 | 337 | |
| ZrCl2 | — | — | — | — | — | 722 | Разл. | — | 74 | -404 | 110 | |
| ZrCl, | Гексагон. | — | — | — | — | — | 770** | — | 98 | -701 | 138 | |
| ZrCl4 | Моноклинная | 0,6361 | 0,7407 | 0,6256 | 109,3 | 437 | 333,6** | 2,80 | 120 | -979,8 | — | |
| ТrOСl2 | Ромбич. | 0,9687 | 1,0589 | 0,9143 | — | — | — | — | — | -1083 | — | |
| ZrBr3 | Гексагон. | — | — | — | — | Разл. | — | — | 99,6 | -636 | 184 | |
| ZrBr4 | Кубич. | 1,095 | — | — | — | 450 | 355** | 3,98 | 125 | -760,6 | 225 | |
| ZrI3 | Гексагон. | — | — | — | — | Разл. | — | — | 104 | -395 | 209 | |
| ZrI4 | Кубич. | 1,179 | — | — | — | 500 | 418** | 4,85 | 123 | -482 | 257 | |
*Т-ра полиморфного перехода. **Т-ра возгонки.
Трихлорид ZrCl3 при нагр. диспропорционирует с выделением ZrCl4 и последоват. образованием ZrCl2,8 (200 °С), ZiCl1,6 (300 °С), ZrCl (450 °С) и Zr (600 °С, вакуум). Тетрахлорид ZrC4: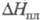 49 кДж/моль,
49 кДж/моль,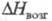 103 кДж/моль; tкрит 503,5 °С, ркрит 5,7 МПа; ур-ние температурной зависимости давления пара lg p (Пa)= 13,8-5700/Т для твердого и lgp (Па) = 11,4 - 3500/Т для жидкого ZrCl4; раств. в этаноле, диэтиловом эфире, образует аддукты с к-тами Льюиса (напр., ZrCl4 * PCl5, ZrCl4*2CH3CN и др.), хлороцирконаты с хлоридами металлов (K2ZrCl6, BaZrCl6 и др.). Получают ZrCl4 взаимод. Zr с С12 или НС1 выше 300 °С, ZrO2 с ССl4 или СОС12 выше 300 °С, смеси ZrO2 и С с С12 выше 600 °С, карбида Zr с С12 выше 400 °С; используют как промежут. продукт в произ-ве Zr, исходное в-во для магниетермич. восстановления, катализатор орг. р-ций (напр., Фриделя-Крафтса). Гексахлороцирконат калия K2ZrCl6, т. пл. 799 °С, т-ра полиморфного перехода 622 °С,
103 кДж/моль; tкрит 503,5 °С, ркрит 5,7 МПа; ур-ние температурной зависимости давления пара lg p (Пa)= 13,8-5700/Т для твердого и lgp (Па) = 11,4 - 3500/Т для жидкого ZrCl4; раств. в этаноле, диэтиловом эфире, образует аддукты с к-тами Льюиса (напр., ZrCl4 * PCl5, ZrCl4*2CH3CN и др.), хлороцирконаты с хлоридами металлов (K2ZrCl6, BaZrCl6 и др.). Получают ZrCl4 взаимод. Zr с С12 или НС1 выше 300 °С, ZrO2 с ССl4 или СОС12 выше 300 °С, смеси ZrO2 и С с С12 выше 600 °С, карбида Zr с С12 выше 400 °С; используют как промежут. продукт в произ-ве Zr, исходное в-во для магниетермич. восстановления, катализатор орг. р-ций (напр., Фриделя-Крафтса). Гексахлороцирконат калия K2ZrCl6, т. пл. 799 °С, т-ра полиморфного перехода 622 °С,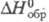 -1932 кДж/моль. Оксихлориды, напр. ZrOCl2, Zr2O3Cl2,- бесцв. кристаллы, при нагр. выше 70 °С в водном р-ре гидролизуются; промежут. продукты хлорирования ZrO2 или гидролиза ZrCl4, образуются также при растворении соед. Zr в соляной к-те. Октагидрат ZrOCl2 * 8Н2О хорошо раств. в воде (67% при 25 °С) и гораздо хуже в соляной к-те, его применяют для получения небольших партий особо чистых соед. Zr перекристаллизацией.
-1932 кДж/моль. Оксихлориды, напр. ZrOCl2, Zr2O3Cl2,- бесцв. кристаллы, при нагр. выше 70 °С в водном р-ре гидролизуются; промежут. продукты хлорирования ZrO2 или гидролиза ZrCl4, образуются также при растворении соед. Zr в соляной к-те. Октагидрат ZrOCl2 * 8Н2О хорошо раств. в воде (67% при 25 °С) и гораздо хуже в соляной к-те, его применяют для получения небольших партий особо чистых соед. Zr перекристаллизацией.
Тетраиодид ZrI4: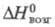 119 кДж/моль; ур-ние температурной зависимости давления пара lg р (Па) = 22,99 -7,680/742,164 lg Т - 1,344 * 10-3 T (298-704 К), в парах выше 1200 °С разлагается до Zr; раств. в этаноле, бензоле; получают взаимод. Zr (реже ZrO2) с I2 при 300-500 °С; промежут.
119 кДж/моль; ур-ние температурной зависимости давления пара lg р (Па) = 22,99 -7,680/742,164 lg Т - 1,344 * 10-3 T (298-704 К), в парах выше 1200 °С разлагается до Zr; раств. в этаноле, бензоле; получают взаимод. Zr (реже ZrO2) с I2 при 300-500 °С; промежут.
продукт при иодидном рафинировании Zr.
Э. Г. Раков.
