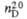Трифторуксусная кислота
ТРИФТОРУКСУСНАЯ КИСЛОТА CF3COOH, мол.м. 114,03; бесцв. дымящая на воздухе жидкость с острым раздражающим запахом; т. пл. -15,3 0C, т. кип. 72,4 0C; 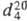 1,489;
1,489; 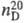 1,2850; tкрит 218,15 0C, ркрит 3,26 МПа,
1,2850; tкрит 218,15 0C, ркрит 3,26 МПа, 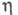 1,225 мПа·с (О 0C), 0,877 мПа·с (20 0C);
1,225 мПа·с (О 0C), 0,877 мПа·с (20 0C); 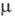 7,6·10-30 Кл·м;
7,6·10-30 Кл·м; 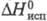 34,21 кДж/моль,
34,21 кДж/моль, 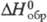 -1020 кДж/моль;
-1020 кДж/моль;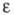 8,55 (20 0C); рКа 0,558 (25 0C, вода).
8,55 (20 0C); рКа 0,558 (25 0C, вода).
Смешивается с водой и орг. р-рителями во всех соотношениях, с водой образует азеотропную смесь (т. кип. 105,46 0C, 79,4% по массе трифторуксусной кислоты). С диалкиловыми эфирами, кетонами, карбоновыми к-тами и др. электронодонорными соед. дает прочные комплексы.
СВОЙСТВА НЕКОТОРЫХ ПРОИЗВОДНЫХ ТРИФТОРУКСУСНОЙ КИСЛОТЫ
| Соединение | Мол. м. | T. пл., :С | T. кип., 0C | | |
| Трифторацетилхлорид CF3COCl | 132,47 | — | 18,5 | — | — |
| Трифторацетангидрид (CF3CO)2O | 210,03 | -65,0 | 38,8-39 | 1,495* | 1,2680* |
| Этилтрифторацетат CF3COOC2H5 | 142,03 | — | 61,0 | 1,464 | 1,2772 |
| Трифторацетамид CF3CONH2 | 113,04 | 74,8 | 162,5 | — | — |
| Трифторацетонитрил CF3CN | 95,02 | -100 | -63 | — | — |
* При 25 0C.
Термически стабильна, не разлагается при нагр. до 400 0C. По хим. св-вам - типичная карбоновая кислота. Свойства производных трифторуксусной кислоты см. в таблице.
Трифторуксусная кислота легко присоединяется по кратным связям алке-нов, циклоалкенов, ацетиленов с образованием трифтораце-татов; с галогенами дает малоустойчивые гипогалогениты CF3COOHaI, к-рые селективно галогенируют разл. соед.; при нагр. Ag-соли трифторуксусной кислоты с избытком I2 образуется трифторметилио-дид; при восстановлении трифторуксусной кислоты и ее эфиров LiAlH4 при О 0C -трифторацетальдегид, а при избытке восстановителя при 30 0C - 2,2,2-трифторэтанол. Р-ция с многоатомными спиртами (напр., с триолами) приводит к полициклич. ортоэфи-рам, напр.:
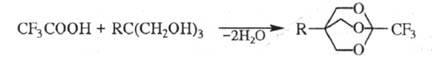
При действии P2O5 на трифторуксусную кислоту образуется трифторацет-ангидрид- сильный ацилирующий агент; при взаимод. со спиртами трифторуксусная кислота дает сложные эфиры, с аминами - амиды, с карбоновыми к-тами - смешанные ангидриды. Последние, а также (CF3CO)2O в присут. минер. K-T или сульфокислот используют в качестве промоторов при ацилировании спиртов, фенолов, тиолов, напр.:
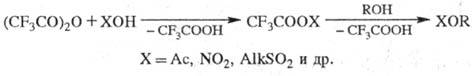
Алкены и нек-рые ароматич. соед. в этих условиях образуют кетоны, напр.:
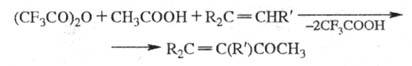
В пром-сти трифторуксусную кислоту получают электрохим. фторировани-ем ангидрида или фторангидрида уксусной к-ты в безводном HF с послед, гидролизом образующегося фторангидрида трифторуксусной кислоты.
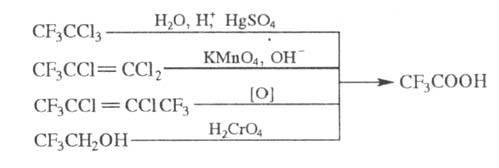
Трифторуксусная кислота может быть получена также кислотным гидролизом 1,1,1-трифтортрихлорэтана, окислением хлоролефинов, содержащих группу CF3, или 2,2,2-трифгорэтанола:
Трифторуксусная кислота - сырье в орг. синтезе, катализатор в р-циях этерифи-кации и полимеризации, р-ритель для ряда термостойких полимеров. Трифгорацетангидрид применяют в произ-ве ацетатного шелка (США, Великобритания), фармацевтич. препаратов, пестицидов, в качестве реагента для защиты функц. групп в синтезе пептидов.
Трифторуксусная кислота - трудногорюча, невзрывоопасна. В жидком виде и в парах вызывает сильные ожоги кожных покровов и слизистых оболочек. ПДК в воздухе рабочей зоны 2 мг/м3.
Лит.: Физер Л., Физер M., Реагенты для органического синтеза, пер. с англ., т. 3, M., 1970; Исикаве H., Кобаяси Ё., Фтор. Химия и применение, пер. с япон., M., 1982; Промышленные фторорганические продукты. Справочник, Л., 1990, с. 367-71. И. И. Крылов.