Биохимические изменения в мышцах при патологии
Общими для большинства заболеваний мышц (прогрессирующие мышечные дистрофии, атрофия мышц в результате их денервации, тенотомия, полимиозит, некоторые авитаминозы и т.д.) являются резкое снижение в мышцах содержания миофибриллярных белков, возрастание концентрации белков стромы и некоторых саркоплазматических белков, в том числе миоальбумина. Наряду с изменениями фракционного состава мышечных белков при поражениях мышц наблюдается снижение уровня АТФ и креа-тинфосфата. Например, через 12 дней после денервации содержание АТФ в денервированной икроножной мышце кролика снижается более чем в 2 раза. Отмечаются также снижение АТФазной активности контрактиль-ных белков (миозина), уменьшение количества имидазолсодержащих ди-пептидов.
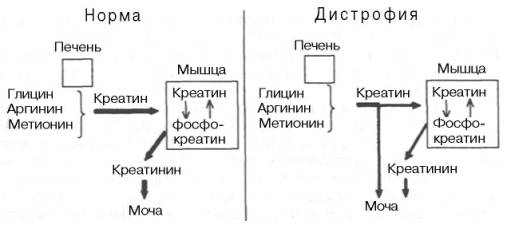
Рис. 20.9. Схематическое изображение происхождения креатинурии при прогрессирующей мышечной дистрофии (по Д.Л. Фердману).
При прогрессирующих мышечных дистрофиях и других заболеваниях, связанных с распадом мышечной ткани, часто отмечаются сдвиги в фос-фолипидном составе мышц: значительно снижается уровень фосфатидил-холина и фосфатидилэтаноламина, концентрация сфингомиелина и лизо-фосфатидилхолина повышается. До сих пор истинные механизмы изменения фосфолипидного состава мышечной ткани при патологии не выяснены, неизвестна также роль этих сдвигов в патогенезе мышечных дистрофий.
Для многих форм патологии мышечной ткани характерны нарушение метаболизма креатина и его усиленное выделение с мочой (креатинурия). Несмотря на многочисленные исследования и обилие фактического материала, вопрос о причинах креатинурии при заболеваниях мышц не может считаться окончательно решенным.
Принято считать, что креатинурия у больных миопатией является результатом нарушения в скелетной мускулатуре процессов фиксации (удержания) креатина и его фосфорилирования. Если нарушен процесс синтеза креатинфосфата, то не образуется и креатинина; содержание последнего в моче резко снижается. В результате креатинурии и нарушения синтеза креатинина резко повышается креатиновый показатель (креа-тин/креатинин) мочи. Данный механизм представлен на рис. 20.9.
При патологии мышечной ткани можно наблюдать определенную закономерность в изменении активности ферментов в мышцах: уменьшается активность ферментов, локализованных в саркоплазме; незначительно изменяется активность ферментов, связанных с митохондриями; заметно возрастает активность лизосомальных ферментов. Наконец, показано, что при многих заболеваниях мышечной системы наступают сдвиги в системе цАМФ: снижается содержание цАМФ в мышечной ткани, повышается активность фосфодиэстеразы и нарушается способность аденилатциклазы активироваться под влиянием адреналина и фторида натрия.
Нарушение метаболизма сердечной мышцы при ишемической болезни сердца. Для ишемизированного миокарда характерны сниженное окислительное фосфорилирование и повышенный анаэробный обмен. Раннее увеличение гликогенолиза и гликолиза за счет имеющегося в сердечной мышце гликогена и глюкозы, усиленно поглощаемой миокардом в начальной стадии ишемии, происходит в результате повышения внутриклеточной концентрации катехоламинов и цАМФ, что в свою очередь стимулирует образование активной формы фосфорилазы – фосфорилазы а и активацию фосфофруктокиназы – ключевого фермента гликолиза. Однако даже максимально усиленный анаэробный метаболизм не способен длительно защищать уже поврежденный гипоксический миокард. Очень скоро запасы гликогена истощаются, гликолиз замедляется вследствие внутриклеточного ацидоза, который ингибирует фосфофруктокиназу.
Содержание АТФ и креатинфосфата в клетке резко снижается в результате нарушения окислительного фосфорилирования в митохондриях. Одно из первых проявлений этого состояния – нарушение мембранной проницаемости. Нарушение целостности мембран способствует выходу из клетки ионов, в том числе ионов К+, а также ферментов. Дефицит энергетических ресурсов и нарушение ионного состава, существенные изменения различных мембранных «резервуаров», обеспечивающих контроль за уровнем внутриклеточного кальция, обусловливают торможение функциональной активности мышечных клеток и их постепенную гибель. В этот же период выявляются изменения состава белков миокарда (резкое снижение содержания миофибриллярных белков и накопление белков стромы). Нарушение обмена углеводов, белков и липидов (свободные жирные кислоты не окисляются, а преимущественно включаются в триглицериды) при инфаркте миокарда находит отражение в жировой инфильтрации сердечной мышцы.
Размер повреждения миокарда при возникновении ишемии, снижение активности ферментов в сердечной мышце и возрастание активности соответствующих ферментов в сыворотке крови (например, креатинкиназы) в значительной мере коррелируют друг с другом. Следует признать, что в диагностике инфаркта миокарда определение активности креатинкиназы, АсАТ и ЛДГ в сыворотке крови – наиболее чувствительные тесты. Повышение активности указанных ферментов, особенно креатинкиназы, является постоянным и наиболее высоким. Важно также исследование в сыворотке крови изоферментных спектров креатинкиназы (повышение активности изофермента MB) и ЛДГ (увеличение активности изоферментов ЛДГ1 и ЛДГ2). В последние годы четко показано, что определение в сыворотке крови миокардиально специфичных белков (миоглобин, тропонин Т и др.) – весьма чувствительный ранний тест повреждения миокарда.


