3.4.1. Электролитная необратимая коагуляция
Критерий устойчивости дисперсных систем, стабилизированных двойными ионными слоями, можно получить из теории ДЛФО при рассмотрении зависимости полной потенциальной энергии взаимодействия частиц от расстояния между ними. Пример таких зависимостей приведен на рис. 2.23.
|
Превышение энергии отталкивания по сравнению энергией притяжения на определенных расстояниях обусловливает возникновение энергетического барьера, при достаточной величине которого (DUe » 10 kT) система будет находиться в устойчивом состоянии, характеризуемом малой вероятностью слипания частиц, так как преодоление этого барьера возможно только для очень активных частиц, обладающих кинетической энергией, большей DUe. В присутствии электролитов, которые подавляют диффузию противоионов в двойном ионном слое и снижают избыточное осмотическое давление, в результате чего понижается потенциальный энергетический барьер, система переходит в неустойчивое состояние. Пример кривой потенциальной энергии взаимодействия частиц в такой астабилизированной системе приведен на рис. 2.23 (кривые 2 и 3). Положение кривой суммарной потенциальной энергии взаимодействия в отрицательной области указывает на тот факт, что любое столкновение частиц способно привести к их слипанию. Таким образом, системы, для которых характерны потенциальные кривые этого типа, не могут существовать, так как в них протекает необратимый процесс коагуляции.
Уменьшение энергетического барьера возможно не только в результате подавления диффузии, но и при специфической адсорбции противоионов, нейтрализующих частично или даже полностью заряд поверхности. В этой связи различают два типа электролитной коагуляции: концентрационную и нейтрализационную.
При рассмотрении устойчивости дисперсных систем величина энергетического барьера, препятствующего коагуляции, должна учитывать как потенциальный максимум, так и потенциальный минимум на кривой потенциальной энергии взаимодействия частиц. DUmaxсчитается равным сумме энергетического барьера отталкивания, расположенного на графике (рис.2.23) в положительной области энергий, и глубины вторичного минимума потенциальной энергии взаимодействия, т.е.
DUmax = DUe + DUm . (2.3.121)
Критическим считается значение DUmax < 10 kT.
Теория ДЛФО позволяет предсказать величину критической концентрации электролита, при которой происходит необратимый процесс коагуляции. Такую концентрацию называют порогом коагуляции.
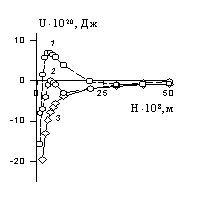 Рис. 2.23. Потенциальная энергия взаимодействия устойчивой (1) и неустойчивых (2, 3) систем
Рис. 2.23. Потенциальная энергия взаимодействия устойчивой (1) и неустойчивых (2, 3) систем