Бромбензолы
БРОМБЕНЗОЛЫ С6Н6_nВrn(n = 1-6). Практич. интерес представляют бромбензол, 1,2- и 1,4-дибромбензолы.
Бромбензол (фенилбромид) С6Н5Вг, мол. м. 157,02; бесцв. жидкость (см. табл.);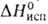 241,28 кДж/кг; не раств. в воде, смешивается с эфиром, хлороформом, бензолом и др. При повыш. т-ре обменивает бром на др. атомы и группы: при взанмод. с NaOH (300-370°С) - на ОН-группу, при нагр. с KCN или CuCN (200°С) - на CN-группу, при р-ции с Na,SO3 или солями жирных к-т (кат. - соли Си; 200 °С) - соотв. на сульфо- или ацильную группу. При нагр. бромбензола с Na в смеси эфира с бензолом образуется дифенил; с Mg легко получается C6H5MgBr (выход 90%), с Li-фениллитий C6H5Li, с HNO3 или Н2SО4 - соотв. бромнитробензолы и бромсульфокислоты.
241,28 кДж/кг; не раств. в воде, смешивается с эфиром, хлороформом, бензолом и др. При повыш. т-ре обменивает бром на др. атомы и группы: при взанмод. с NaOH (300-370°С) - на ОН-группу, при нагр. с KCN или CuCN (200°С) - на CN-группу, при р-ции с Na,SO3 или солями жирных к-т (кат. - соли Си; 200 °С) - соотв. на сульфо- или ацильную группу. При нагр. бромбензола с Na в смеси эфира с бензолом образуется дифенил; с Mg легко получается C6H5MgBr (выход 90%), с Li-фениллитий C6H5Li, с HNO3 или Н2SО4 - соотв. бромнитробензолы и бромсульфокислоты.
СВОЙСТВА БРОМБЕНЗОЛОВ

Дибромбензолы С6Н4Вr2, мол. м. 235,92; не раств. в воде, раств. в спиртах, эфирах, ацетоне, CS2 и др.
В пром-сти бромбензол получают жидкофазным бромированием бензола на холоду в присут. железных стружек (побочные продукты - 1,2 и 1,4-дибромбензолы); при избытке брома получают дибромбензолы. Бромбензол -р-ритель; применяется для получения реактива Гриньяра, дифенила и др.; 1,2-дибромбензол - трансформаторное масло, р-ритель жиров, восков; 1,4-дибромбензол используется для синтеза красителей, лек. ср-в и др. Г.В.Моцарев.
Комментарии*
Бромбензолы — ароматические соединения общей формулы C₆H₆₋ₙBrₙ (n = 1–6). Наибольшее практическое значение имеют бромбензол, 1,2- и 1,4-дибромбензолы.
Бромбензол (фенилбромид) C₆H₅Br, мол. масса 157,02; бесцветная жидкость; ΔHисп 241,28 кДж/кг; не растворяется в воде, смешивается с эфиром, хлороформом, бензолом и другими органическими растворителями. При повышенных температурах активно вступает в реакции нуклеофильного замещения, обменивая бром на другие атомы и группы: при взаимодействии с NaOH (300–370°C) — на ОН-группу, при нагревании с KCN или CuCN (200°C) — на CN-группу, при реакции с Na₂SO₃ или солями жирных кислот (катализатор — соли Cu; 200°C) — соответственно на сульфо- или ацильную группу. При нагревании бромбензола с Na в смеси эфира с бензолом образуется дифенил; с Mg легко получается C₆H₅MgBr (выход 90%), с Li — фениллитий C₆H₅Li, с HNO₃ или H₂SO₄ — соответственно бромнитробензолы и бромсульфокислоты.
Дибромбензолы C₆H₄Br₂, мол. масса 235,92; не растворяются в воде, растворяются в спиртах, эфирах, ацетоне, CS₂ и других органических растворителях.
В промышленности бромбензол получают жидкофазным бромированием бензола на холоду в присутствии железных стружек (побочные продукты — 1,2- и 1,4-дибромбензолы); при избытке брома получают дибромбензолы. Бромбензол — растворитель; применяется для получения реактива Гриньяра, дифенила и других соединений; 1,2-дибромбензол — трансформаторное масло, растворитель жиров, восков; 1,4-дибромбензол используется для синтеза красителей, лекарственных средств и других продуктов.
Дополнения:
- Бромбензолы являются классическими субстратами в реакциях металло-органического синтеза, особенно в реакциях кросс-сочетания (например, реакции Сузуки, Стилла, Негиши)
- 1,4-Дибромбензол служит важным мономером в синтезе полимеров и жидкокристаллических материалов
- Бромбензолы проявляют токсические свойства, бромбензол обладает гепатотоксическим действием
- Орто- и пара-дибромбензолы различаются по физическим свойствам: пара-изомер имеет более высокую температуру плавления (87°C) по сравнению с орто-изомером (7°C)
- В современных методах синтеза бромбензолы часто получают каталитическим бромированием с использованием N-бромсукцинимида
*Подобраны с помощью LLM, верифицированы, но возможны неточности.
Синонимы/примеры:*
Бромбензол; Фенилбромид; Монобромбензол
*подобраны ИИ, возможны неточности
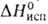 241,28 кДж/кг; не раств. в воде, смешивается с эфиром, хлороформом, бензолом и др. При повыш. т-ре обменивает бром на др. атомы и группы: при взанмод. с NaOH (300-370°С) - на ОН-группу, при нагр. с KCN или CuCN (200°С) - на CN-группу, при р-ции с Na,SO3 или солями жирных к-т (кат. - соли Си; 200 °С) - соотв. на сульфо- или ацильную группу. При нагр. бромбензола с Na в смеси эфира с бензолом образуется дифенил; с Mg легко получается C6H5MgBr (выход 90%), с Li-фениллитий C6H5Li, с HNO3 или Н2SО4 - соотв. бромнитробензолы и бромсульфокислоты.
241,28 кДж/кг; не раств. в воде, смешивается с эфиром, хлороформом, бензолом и др. При повыш. т-ре обменивает бром на др. атомы и группы: при взанмод. с NaOH (300-370°С) - на ОН-группу, при нагр. с KCN или CuCN (200°С) - на CN-группу, при р-ции с Na,SO3 или солями жирных к-т (кат. - соли Си; 200 °С) - соотв. на сульфо- или ацильную группу. При нагр. бромбензола с Na в смеси эфира с бензолом образуется дифенил; с Mg легко получается C6H5MgBr (выход 90%), с Li-фениллитий C6H5Li, с HNO3 или Н2SО4 - соотв. бромнитробензолы и бромсульфокислоты. 

Бромбензолы — ароматические соединения общей формулы C₆H₆₋ₙBrₙ (n = 1–6). Наибольшее практическое значение имеют бромбензол, 1,2- и 1,4-дибромбензолы.
Бромбензол (фенилбромид) C₆H₅Br, мол. масса 157,02; бесцветная жидкость; ΔHисп 241,28 кДж/кг; не растворяется в воде, смешивается с эфиром, хлороформом, бензолом и другими органическими растворителями. При повышенных температурах активно вступает в реакции нуклеофильного замещения, обменивая бром на другие атомы и группы: при взаимодействии с NaOH (300–370°C) — на ОН-группу, при нагревании с KCN или CuCN (200°C) — на CN-группу, при реакции с Na₂SO₃ или солями жирных кислот (катализатор — соли Cu; 200°C) — соответственно на сульфо- или ацильную группу. При нагревании бромбензола с Na в смеси эфира с бензолом образуется дифенил; с Mg легко получается C₆H₅MgBr (выход 90%), с Li — фениллитий C₆H₅Li, с HNO₃ или H₂SO₄ — соответственно бромнитробензолы и бромсульфокислоты.
Дибромбензолы C₆H₄Br₂, мол. масса 235,92; не растворяются в воде, растворяются в спиртах, эфирах, ацетоне, CS₂ и других органических растворителях.
В промышленности бромбензол получают жидкофазным бромированием бензола на холоду в присутствии железных стружек (побочные продукты — 1,2- и 1,4-дибромбензолы); при избытке брома получают дибромбензолы. Бромбензол — растворитель; применяется для получения реактива Гриньяра, дифенила и других соединений; 1,2-дибромбензол — трансформаторное масло, растворитель жиров, восков; 1,4-дибромбензол используется для синтеза красителей, лекарственных средств и других продуктов.
Дополнения: