Бориды
БОРИДЫ, соед. бора с металлами. Известны для большинства элементов подгрупп Ia-IIа и IIIб-VIIIб, а также А1; для нек-рых элементов подгрупп Iб-IIб известны бинарные системы с высоким содержанием В (напр., СuВ22, ZnB22), к-рые относят не к хим. соединениям, а к твердым р-рам. Один металл может образовывать неск. боридов разного состава. Различают богатые металлом низшие бориды (М3В, М2В, М3В2, MB, M3B4) и богатые бором высшие бориды (МВ2, МВ4, МВ6, МВ12 и др.).
Названия боридов включают название металла с приставкой, указывающей число атомов металла в ф-ле, и слово "борид" с обозначением числа атомов В, напр. W2В5-пентаборид дивольфрама.
СВОЙСТВА БОРИДОВ МЕТАЛЛОВ 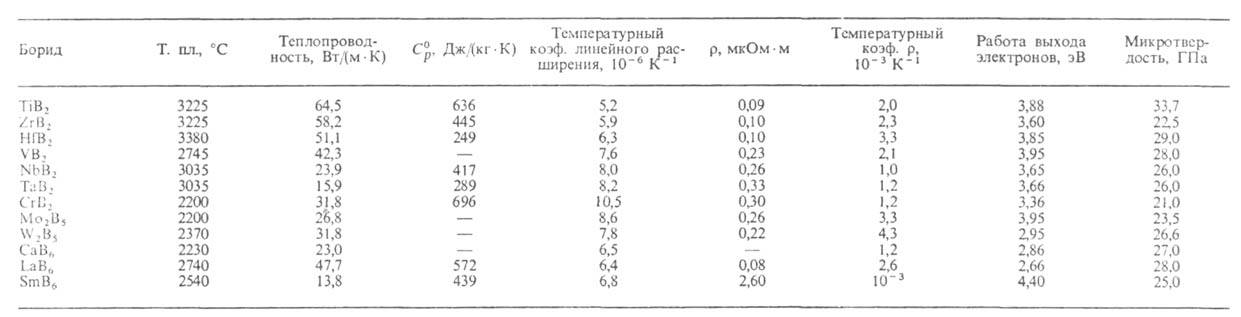
Взаимод. между атомами металла и бора в боридах относительно слабое, поэтому их структуру рассматривают как две слабо связанные подрешетки. Структура низших боридов определяется металлич. подрешеткой, высших - борной. В соединениях типа М4В и М2В атомы В изолированы друг от друга, в соединениях типа MB они образуют одинарные зигзагообразные цепи, в М3В4 - сдвоенные цепи. По мере увеличения содержания В структура боридов существенно усложняется. Так, в МВ2 атомы В образуют плоские сетки, в МВ4 - гофрированные сетки и каркасы в виде окгаэдрич. группировок, в МВ6 - октаэдры, в МВ12 - кубооктаэдры и икосаэдры, в МВ66 - цепи икосаэдров. Гексаген, кристаллич. решетка характерна для МВ2 и МВ4, тетрагональная-для МВ2, MB и МВ4, кубическая - для М2В, MB, MB6, МВ12, МВ66, ромбическая-для М4В, MB, M3B4, М4В, МВ12.
В молекулах боридов борные группировки, в к-рых связь В—В ковалентная, электронодефицитны; для их стабилизации необходимо привлечение электронов от атома металла. В результате между металлом и бором осуществляются связи промежут. типа: у боридов элементов III-VIII групп, отдающих более двух электронов, они частично металлические, в остальных случаях - частично ионные. С возрастанием содержания бора в пределах бинарной системы растет доля ковалентных связей В—В и уменьшается взаимод. металл - бор, в результате чего повышаются твердость, т-ра плавления, теплопроводность и электрич. проводимость и уменьшается температурный коэф. линейного расширения. Одновременно возрастает хим. стойкость. Напр., при изменении состава от Nb3B2 до NbB2 т-ра плавления увеличивается от 1860 до 3035 °С, температурный коэф. линейного расширения уменьшается от 13,8*10-б до 8,0*10-6 К-1.
Бориды устойчивы к действию воды (кроме низших боридов Be и Mg), соляной, фтористоводородной и карбоновых к-т. Легко разлагаются HNO3 и H2SO4 при нагревании. Взаимод. с расплавами щелочей, карбонатов и сульфатов щелочных металлов. При окислении на воздухе образуют оксиды металла и бора, причем на пов-сти боридов формируются пленки пироборатов, обладающие защитными св-вами. Бо-риды Ti и Zr устойчивы к действию расплавов металлов.
Бориды не разлагаются в вакууме при нагревании до их т-р плавления. При испарении диссоциируют на элементы. Бориды металлов I и II групп, а также других в степени окисления + 1 и +2, обладают типично полупроводниковыми св-вами. Бориды металлов в высших степенях окисления по электрич. проводимости, как правило, значительно превосходят соответствующие металлы. Наиб. термич. стабильностью,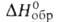 и микротвердостью обладают соед. металлов III и IV групп.
и микротвердостью обладают соед. металлов III и IV групп.
Осн. способы получения боридов: 1) взаимод. металла с В с использованием внеш. нагрева (спекание, сплавление) либо инициированием внеш. источником тепла с послед. разогревом реагентов благодаря выделению теплоты р-ции (самораспространяющийся высокотемпературный синтез). Образующиеся бориды имеют вид спеков, требующих размола; 2) восстановление оксида металла смесью В и С, карбидом бора или бором при 1500-2000°С в вакууме. Бориды получаются в виде порошков с размером частиц 1-40 мкм; 3) электролиз расплавов боратов и оксидов металлов (лаб. способ). Образуются монокристаллы размером до 1 мм; 4) взаимод. металл- и борсодержащих соед. в условиях низкотемпературной плазмы. Образуются порошки с размером частиц 50-100 нм.
Монокристаллы боридов размером до 5 мм получают кристаллизацией из р-ров бора и металлов в расплавах Al, Zn, крупные монокристаллы диаметром до 20 и длиной до 100 мм - методами зонной плавки, Вернейля.
Изделия из порошков боридов изготавливают спеканием предварительно спрессованных заготовок или горячим прессованием. Покрытия из боридов на разл. подложках получают методом осаждения из газовой фазы при взаимод. галогенидов металлов и бора, плазменного напыления порошков и др.
Ниже описаны важнейшие представители боридов (см. табл.). Диборид титана TiB2 - черные кристаллы с гексагон. решеткой (а = 0,3026 нм, с = 0,3313 нм). Используют для изготовления испарителей для расплавов металлов и футеровки электролизеров, как компонент жаропрочных сплавов, инструментальных материалов, износостойких наплавочных покрытий [в осн. в виде двойного борида - (Ti,Cr)B2].
Диборид циркония ZrB2 - серые кристаллы с гексагон. решеткой (а = 0,1368 нм, с = 0,3528 нм). Устойчив в расплавах цветных и черных металлов, металлургич. шлаков. Характеризуется стабильностью термоэлектрич. св-в (коэф. термоэдс 1,2 мкВ/К). Используют для изготовления защитных чехлов и элементов термопар (в паре с графитом), как нейтронопоглощающий материал для ядерных реакторов и компонент жаропрочных сплавов.
Диборид хрома СгВ2 - серые кристаллы с гексагон. решеткой (а = 0,2970 нм, с = 0,3074 нм). Обладает высокой износостойкостью; компонент износостойких наплавочных покрытий.
Гексаборид лантана LaB6 - фиолетово-пурпурные кристаллы с кубич. решеткой (а = 0,4156 нм). Обладает хорошими термоэмиссионными св-вами. Устойчив к ионной бомбардировке и в агрессивных газовых средах. Применяют в кач-ве эмиттеров в электроннолучевых устройствах средней и высокой мощности.
Гексаборид кальция СаВ6 - черные кристаллы с кубич. решеткой (а = 0,4145 нм). Используют как абразив, нейтронопоглощающий материал.
Литература
Самсонов Г. В., Серебрякова Т.Н., Неронов В. А., Бориды, М, 1975 (Библ.): Boron and refractory borides, ed. by V. I. Matkovich, B.-[a.o.], 1977. A.H. Пилянкевич, Ю. Б. Падерно.
