Ртути халькогениды
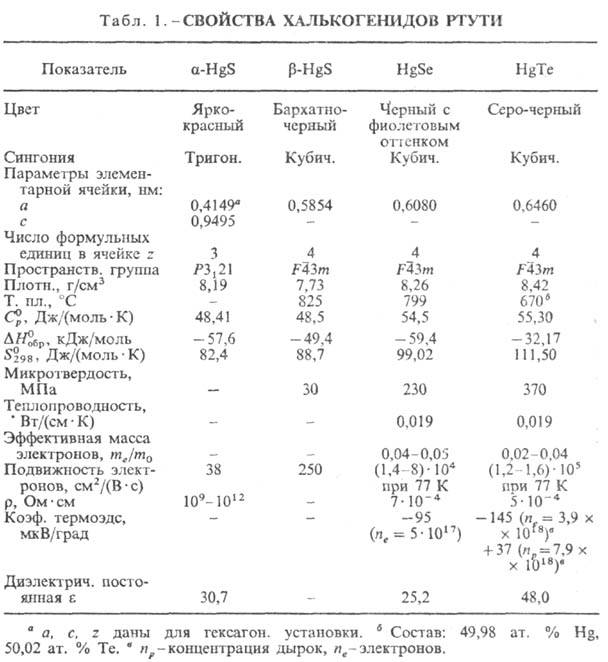
РТУТИ ХАЛЬКОГЕНИДЫ, соед. Hg с S, Se, Те общей ф-лы HgX (табл. 1). Сульфид HgS существует в двух модификациях-a (киноварь) и b (метациннабарит); т-ра перехода a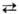 b 345 °С, АН перехода 14,6 кДж/моль. b-HgS, HgSe, HgTe кристаллизуются в решетке типа сфалерита, при давлении 1,5-2,0 ГПа HgSe и HgTe имеют кристаллич. решетку типа a-HgS.
b 345 °С, АН перехода 14,6 кДж/моль. b-HgS, HgSe, HgTe кристаллизуются в решетке типа сфалерита, при давлении 1,5-2,0 ГПа HgSe и HgTe имеют кристаллич. решетку типа a-HgS.
Ртути халькогениды-нестехиометрич. соединения. Область гомогенности HgSe 49,99-50,00 ат.% Hg при 280 °С (по др. данным наблюдается отклонение от стехиометрии в сторону большего содержания Hg). Область гомогенности HgTe 49,40-49,95 ат.% Hg при 400 °С, 49,40-50,009 ат.% Hg при 353 °С. Для ртути халькогенидов преобладающие типы дефектов - вакансии Hg, халькогенов, атомы Hg в межузельном пространстве.
Теллурид-полупроводник р- и n-типа, HgSe, HgS-n-типа. Ртути халькогениды обладают уникальными физ. св-вами. HgTe имеет практически нулевую запрещенную зону (величина перекрывания валентной зоны и зоны проводимости 0,001 эВ, для HgSe эта величина 0,07 эВ). Для a-HgS ширина запрещенной зоны 2,0 эВ.
Ртути халькогениды практически не раств. в воде, орг. р-рителях, разб. к-тах, разлагаются царской водкой. HgS реагирует с конц. р-рами сульфидов щелочных металлов с образованием тиосолей М2HgS2, что используют для извлечения Hg из сульфидных руд.
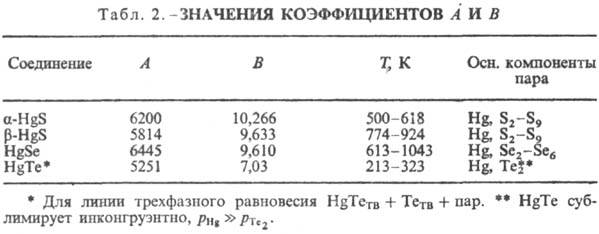
При натр. в вакууме ртути халькогениды легко испаряются, диссоциируя на Hg и X, доля молекул HgX в паре ок. 1·10-4; ур-ние температурной зависимости давления пара HgX: lgp (мм рт.ст.) = -А/Т+ В (табл. 2)
При нагр. на воздухе ртути халькогениды реагируют с О2; по р-ции HgS + О2 : Hg + SO2 в пром-сти получают Hg из киновари. С галогенидами HgHal2 ртути халькогениды образуют соед. Hg3X2Hal2, с халькогенидами Al, Ga, In-полупроводниковые соед. типа HgM2X4. На основе ртути халькогенидов получают твердые р-ры типа Hg1-xМxX, HgTe1-xXx, HgSe1-xXx, где M-Zn, Cd, Мn и др., x-содержание X в атомных долях. Многие из этих р-ров - бесщелевые полупроводники, применяют Нg1-xСdxTе.
Ртути халькогениды получают взаимод. Hg и халькогена при нагр. в запаянных вакуумир. кварцевых ампулах, монокристаллы -сублимацией или выращиванием из нестехиометрич. расплавов HgX в ртути, a-HgS - растиранием Hg с S, a-HgS и b-HgS осаждением из водных р-ров солей Hg.
В природе киноварь - осн. минерал ртути; известны и редкие минералы - метациннабарит, тиманит HgSe, колорадоит HgTe.
Прир. киноварь-осн. пром. сырье в произ-ве Hg. Сульфид HgS-материал для фоторезисторов, катализатор, пигмент, компонент светосоставов на основе CdS; HgSe - материал для фоторезисторов, датчиков для измерения магн. полей; HgTe-компонент материалов для приемников ИК излучения.
Ртути халькогениды токсичны, особенно их аэрозоли и р-ры.
Лит.: Полупроводниковые халькогениды и сплавы на их основе, М., 1975, с. 48-82. И. Н. Один.
