Биосинтез пиримидиновых нуклеотидов
Механизм синтеза пиримидиновых нуклеотидов почти полностью расшифрован благодаря исследованиям П. Рейхарда. Показано, что в клетках животных и в микроорганизмах конечными продуктами синтеза также не являются свободные пиримидиновые основания и остаток рибозы присоединяется к уже сформировавшемуся пиримидиновому кольцу. Синтез начинается с элементарных уровней (СО2, NH3, аспартат), и специфическую ключевую роль выполняет оротовая кислота.
Последовательность химических реакций синтеза пиримидиновых нуклеотидов, в частности УМФ, можно представить в следующем виде:
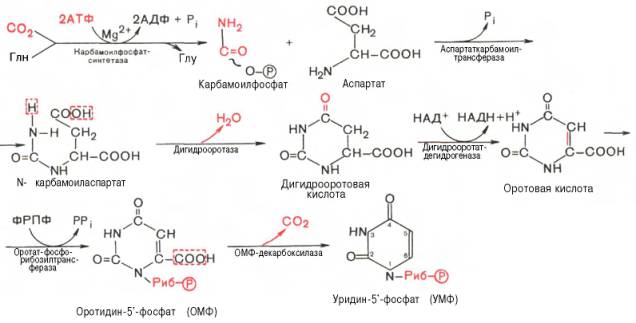
Как видно, I стадия синтеза УМФ включает катализируемое цито-плазматической карбамоилфосфатсинтетазой образование карбамоилфос-фата из глутамина (см. главу 12).
На II стадии карбамоилфосфат реагирует с аспартатом, в результате чего образуется N-карбамоиласпарагиновая кислота. Последняя подвергается циклизации (под действием дигидрооротазы) с отщеплением молекулы воды, при этом образуется дигидрооротовая кислота, которая, подвергаясь дегидрированию, превращается в оротовую кислоту. В этой реакции участвует специфический НАД-содержащий фермент дигидро-оротатдегидрогеназа. Оротовая кислота обратимо реагирует с ФРПФ, являющимся донатором рибозо-фосфата, с образованием оротидин-5'-фос-фата (ОМФ). Декарбоксилирование последнего приводит к образованию первого пиримидинового нуклеотида – уридин-5-фосфата (УМФ).
Превращение УМФ в УДФ и УТФ осуществляется, как и пуриновых нуклеотидов, путем фосфотрансферазных реакций:
УМФ + АТФ <=> УДФ + АДФ ;
УДФ + АТФ <=> УТФ + АДФ.
Биосинтез цитидиловых нуклеотидов. Предшественником цитидиловых нуклеотидов является УТФ, который превращается в ЦТФ:
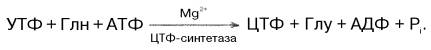
У прокариот в этой реакции используется преимущественно свободный аммиак, в то время как в клетках животных ЦТФ-синтетаза катализирует включение амидной группы глутамина в 4-е положение пиримидинового кольца УТФ. Следует отметить, что образующийся ЦТФ служит отрицательным эффектором регуляторного аллостерического фермента ас-партаткарбамоилтрансферазы, ингибируя по типу обратной связи начальную стадию биосинтеза пиридиновых нуклеотидов. АТФ предотвращает это ингибирование.
Биосинтез тимидиловых нуклеотидов. Тимидиловые нуклеотиды входят в состав ДНК, содержащей дезоксирибозу. Поэтому сначала рассмотрим механизмы синтеза дезоксирибонуклеотидов. При помощи метода меченых атомов было показано, что этот синтез начинается не со свободной дезоксирибозы, а путем прямого восстановления рибонуклеотидов у 2'-го атома углерода. При инкубации меченых предшественников (рибонуклео-тидов) в бесклеточной системе бактерий метку обнаружили в составе дезоксирибонуклеотидов. По данным П. Рейхарда, у Е. coli все 4 рибо-нуклеозиддифосфата восстанавливаются в соответствующие дезоксиана-логи: dАДФ, dГДФ, dЦДФ, dУДФ – при участии сложной ферментной системы, состоящей по меньшей мере из четырех разных ферментов.
Химический смысл превращения рибонуклеотидов в дезоксирибо-нуклеотиды сводится к элементарному акту – восстановлению рибозы в 2-дезоксирибозу, требующему наличия двух атомов водорода. Непосредственным источником последних оказался восстановленный термостабильный белок тиоредоксин, содержащий две свободные SH-группы на 108 аминокислотных остатков. Тиоредоксин легко окисляется, превращаясь в дисульфидную S-S-форму. Для его восстановления в системе имеется специфический ФАД-содержащий фермент тиоредоксинредуктаза (мол. масса 68000), требующая наличия восстановленного НАДФН. Обозначив условно рибонуклеозиддифосфат РДФ, образование дезоксирибонуклеотидов можно представить следующим образом:
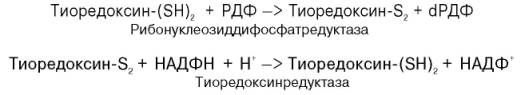
Обе стадии могут быть представлены в виде схемы:
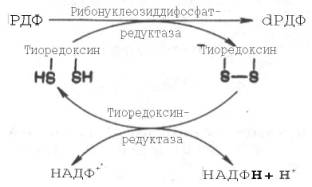
Для синтеза тимидиловых нуклеотидов, помимо дезоксирибозы, требуется также метилированное производное урацила – тимин. Оказалось, что в клетках имеется особый фермент тимидилатсинтаза, катализирующая метилирование не свободного урацила, а dУМФ; реакция протекает по уравнению:
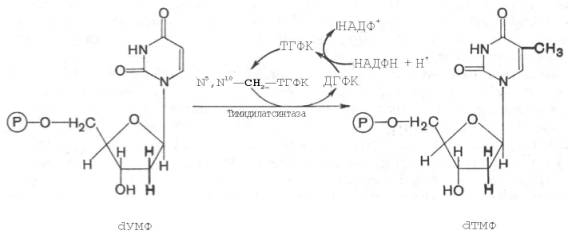
Донором метильной группы в тимидилатсинтазной реакции является N5,N10-метилен-ТГФК, которая одновременно отдает и водородный протон, поэтому одним из конечных продуктов реакции является не тетра-гидро-, а дигидрофолиевая кислота (ДГФК). Последняя вновь восстанавливается до ТГФК под действием НАДФН-зависимой дигидрофолат-редуктазы. Из образовавшегося ТМФ путем фосфотрансферазных реакций образуются dТДФ и dTТФ.
Регенерация N5,N10–СН2–ТГФК, собственно ее биосинтез, представляет определенный интерес. Оказалось, что этот синтез требует участия аминокислоты серина (донатор метильной группы) и пиридоксальфосфат-содержащего фермента сериноксиметилтрансферазы в соответствии с уравнением:
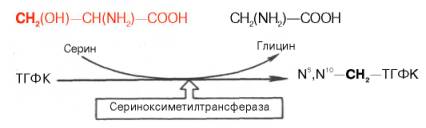
Синтез всех остальных дезоксирибонуклеозид-5'-трифосфатов, непосредственно участвующих в синтезе ДНК, также осуществляется путем фосфорилирования дезоксирибонуклеозид-5'-дифосфатов в присутствии АТФ:
АТФ + dАДФ –> АДФ + dATФ; АТФ + dЦДФ –> АДФ + dЦТФ;
АТФ + dГДФ –> АДФ + dГТФ; АТФ + dТДФ –> АДФ + dТТФ.
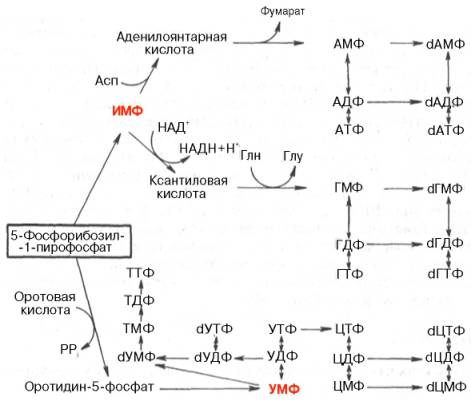
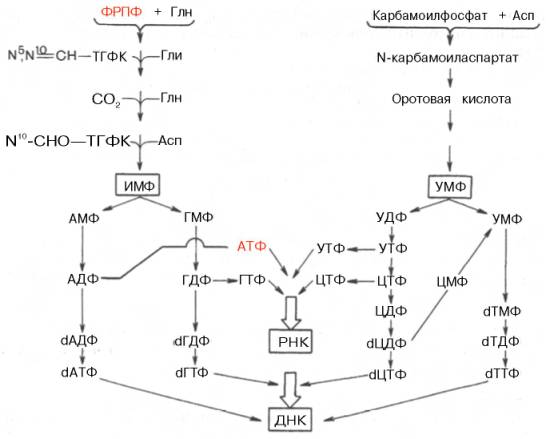
Далее на двух схемах суммированы данные о взаимопревращениях пуриновых и пиримидиновых нуклеотидов, а также о связи их с синтезом нуклеиновых кислот. Как видно из схем, в образовании пуриновых и пиримидиновых нуклеотидов специфическое участие принимает ФРПФ, являющийся донором фосфорибозильного остатка в биосинтезе как оро-тидин-5'-фосфата, так и ИМФ; последние считаются ключевыми субстратами в синтезе нуклеиновых кислот в клетках.