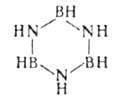
БОРАЗОЛ (боразин, триборинтриимид), мол. м. 80,05; бесцв. жидкость.
Боразол иногда наз. неорг. бензолом. Т. пл. -57°С, т. кип. 55 °С; tкрит
252 °С; плотн. 0,81 г/см3 (55°С), 1,0 г/см* (-57°С); Н°обр
— 548 кДж/моль (газа — 518.74 кДж/моль); nD201,3821;
Н°обр
— 548 кДж/моль (газа — 518.74 кДж/моль); nD201,3821; 2,424*10-4Н/см (7°С), 3,11*10-4 Н/см ( - 57 °С).
Ур-ния температурной зависимости давления пара: lg p(мм рт. ст.)= -1565/Т+7,6616
(258-293 К); lgp(мм рт. ст.) = = 1538/Т + 7,5668 (293-323 К). Боразол раств.
в воде (с медленным разложением до Н2, NH3 и Н3ВО3),
многих орг. р-рителях. Устойчив в течение неск. месяцев в отсутствие влаги,
при длительном хранении разлагается (иногда со взрывом). Разложение ускоряется
под действием света и в присут. примесей. При пиролизе боразола ок. 300°С образуется
BN.
2,424*10-4Н/см (7°С), 3,11*10-4 Н/см ( - 57 °С).
Ур-ния температурной зависимости давления пара: lg p(мм рт. ст.)= -1565/Т+7,6616
(258-293 К); lgp(мм рт. ст.) = = 1538/Т + 7,5668 (293-323 К). Боразол раств.
в воде (с медленным разложением до Н2, NH3 и Н3ВО3),
многих орг. р-рителях. Устойчив в течение неск. месяцев в отсутствие влаги,
при длительном хранении разлагается (иногда со взрывом). Разложение ускоряется
под действием света и в присут. примесей. При пиролизе боразола ок. 300°С образуется
BN.
При комнатной т-ре боразол не окисляется действием О2, в электрич. разряде в смеси с О2 взрывается. Ниже 0°С дает аддукты с водой, спиртами, галогеноводородами и Вг2 состава 1 :3, с С12 и Вг2-состава 1 :2. В присут. катализатора гидрируется с разрушением цикла и образованием NH3 и полимеров. С бензолом в присут. А1С13 дает В-трифенил-боразол. Атомы Н у бора способны замещаться без разрушения цикла. Так, при действии ВС13 или ВВг3 на боразол при повышенной т-ре образуются В-тригалогенборазолы B3N3H3Hal3 - твердые устойчивые соед.; они м. б. также получены по р-ции:
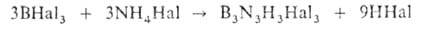
Атомы Н, связанные с азотом, не способны к р-циям замещения. При действии
на боразол ND3, DC1 и DCN замещаются на дейтерий атомы Н, связанные
с азотом, а при действии D2, Na [BD4] или B2D6
- атомы Н, связанные с бором. Наиб, удобный метод синтеза боразола:
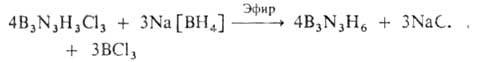
Его выделяют также из смеси продуктов р-ции В2Н6 с
NH3(3B2H6 + 6NH3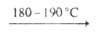 2B3N3H6 + 12Н2), а также получают
взаимод. борогидридов щелочных металлов с NH4Cl напр.:
2B3N3H6 + 12Н2), а также получают
взаимод. борогидридов щелочных металлов с NH4Cl напр.:
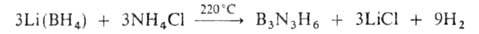
N-Алкил- и N-арилборазолы синтезируют, напр., по р-циям:
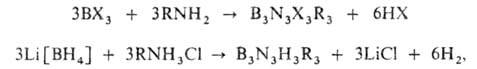
где Х - галоген, алкил, R-алкил, арил. Орг. производные B3N3R3R3,
где R и R' - алкил, арил, получают след. способами:
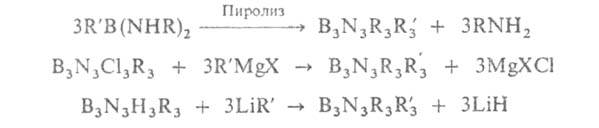
Качественно боразол обнаруживают спектральными методами. Количественно его определяют путем гидролитич. разложения с послед. определением Н3ВО3 и NH3.
Боразол используют для получения BN, его орг. производные - для синтеза термостойких полимеров. Напр., при пиролизе N-трифенилборазола образуется полимер состава [—(C6H5)3N3B3H—]23, в к-ром боразольные циклы связаны через атомы бора. Известны полимеры на основе алкил- или арилпроизводных боразола, содержащие в молекуле алкиленовые, силоксановые, карборановые и др. фрагменты, напр. [(CH3)3N3B3(CH2)6—]14, устойчивые при 400-600 °С
Боразол горюч, с воздухом образует взрывоопасные смеси.
===
Исп. литература для статьи «БОРАЗОЛ»: Джерард В., Химия органических соединений бора, пер. с
англ., М., 1966; Ниденцу К., Даусон Дж., Химия боразотных соединений, пер.
с англ., М., 1968; Коршак В. В., Замятина В. А., Бекасова Н. И., Борорганические
полимеры, М., 1975; Greenwood N. N., в кн.: Comprehensive inorganic chemistry,
v. 8, Oxf.-[a.o.], 1975, p. 665-991. Н.Т. Кузнецов.
Страница «БОРАЗОЛ» подготовлена по материалам химической энциклопедии.