ФОСФИНАЛКИЛЕНЫ (алкилиденфосфораны,
илиды фосфора, реактивы Виттига), соед. общей ф-лы R3P = CR1R2,
где R = AIk, Ar; R1, R2 = H, AIk, Hal, COOR3
и др. Часто к фосфиналкиленам относят близкие по структуре соед. с R = Hal, OR', NR'2.
Более точно строение фосфиналкиленов может быть описано резонансными структурами I и П (см.
также Илиды):

Большинство фосфиналкиленов- кристаллич.
соед. (табл.); раств. в орг. р-рителях, многие фосфиналкилены разлагаются водой. Фосфиналкилены- полярные
(m 1,7 · 10-29-2,3 · 10-29 кл · м), сильноосновные
в-ва (образуют соли с к-тами HHaI и комплексы с к-тами Льюиса). Порядок связи
Р = С в молекуле с несопряженными связями ок. 1,3. В ИК спектре полоса поглощения
связи P = C находится в области 900 см-1; в УФ спектре обычно наблюдаются
две полосы поглощения (lмакс 265 и 340-400 нм). В спектре ЯМР хим.
сдвиги 31P в области 0-80 м. д.
| СВОЙСТВА НЕКОТОРЫХ
ФОСФИНАЛКИЛЕНОВ |
|||
|
Соединение |
T. пл., 0C |
T. кип., °С/мм
рт. ст. |
Хим. сдвиги в спектре
ЯМР31Р (относительно 85%-нойН3РО4),
м.д. |
|
(CH3)3P
= CH2 |
13-14 |
118-120/750 |
21 |
|
(C4H9)3P
= CH2 |
— |
58/0,001 |
16 |
|
Ph3P
= CH2 |
96 |
— |
20 |
|
Ph3P
= CHCN |
190 |
— |
23 |
|
(CH3)3P
= CHSi(CH3)3 |
-36 |
66/11 |
11 |
|
(СН3)3Р
= С[Si(CH3)3]2 |
14-18 |
60/1 |
0 |
|
Ph3P
= C = C = O |
173 |
— |
2,6 |
|
Ph3P
= C = C = S |
225 |
— |
7,7 |
Фосфиналкилены относительно устойчивы
к нагреванию. Соед. с R = AIk перегоняются в вакууме, большинство фосфиналкиленов, стабилизированных
сопряжением, разлагается лишь выше 200 0C. Фосфиналкилены сравнительно легко
окисляются и гидролизуются, давая соответствующие фосфиноксиды;
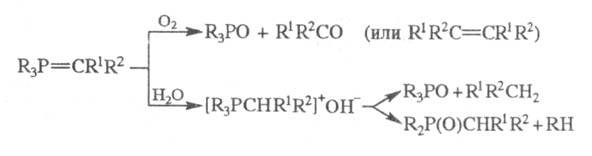
При действии AlHn(OR)4_n
(п= 1-4) фосфиналкилены восстанавливаются до соед. Р(III). Алкилгалогениды алкилируют
фосфиналкилены по метиле-новому атому С.
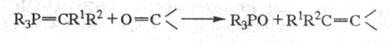
Наиб. изучена р-ция фосфиналкиленов
с карбонильными соед. (см. Виттига реакция), протекающая по схеме:
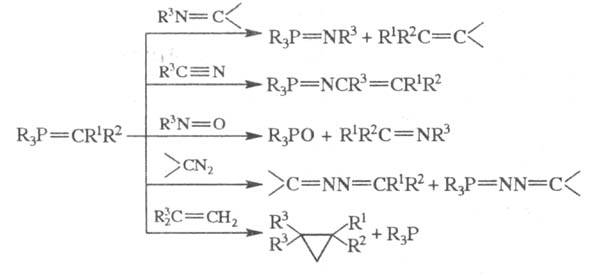
Фосфиналкилены активно взаимод. со
многими др. соед., содержащими активированные кратные связи, напр.:
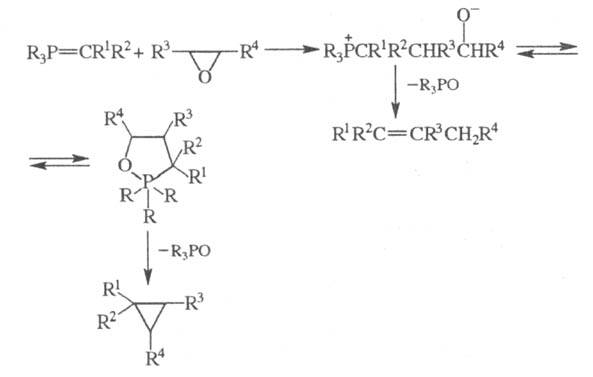
В р-циях фосфиналкиленов с оксиранами
образуются производные циклопропана (наряду с олефинами):
Осн. метод получения фосфиналкиленов-
разложение солей фосфония в присут. оснований В (щелочной металл, RLi, RONa,
NaOH, NR3 и др.):
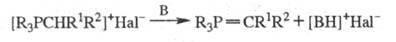
Др. методы получения:
1) присоединение карбенов
к третичным фосфинам;
2) взаимод. галогенфосфоранов
с соед., содержащими активную метиленовую группу, напр.:
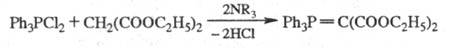
3) р-ция фосфинов с соед.
с активир. связью C = C.
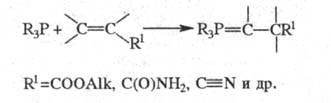
Фосфиналкилены используют в препаративной
практике для получения соед. сложного строения со связью C = C, напр. стероидов,
каротиноидов.
Лит.: Коrбридж
Д., Фосфор, пер. с англ., M., 1982, с. 219-29; Общая органическая химия, пер.
с англ., т. 5, M., 1983, с. 108-29; Bestmann H., Zimmermann R., в кн.: Organic
phosphorus compounds, v. 3, N. Y., 1972, p. 3-184; Trippett S., в кн.: Organophosphorus
chemistry, v. 3, L., 1972, p. 150. Г. И. Дрозд.