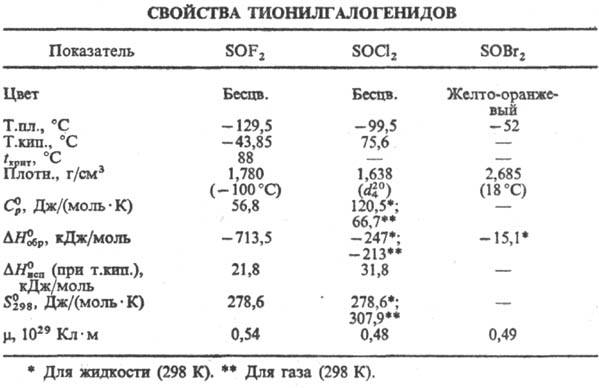
ТИОНИЛГАЛОГЕНИДЫ [дигалогениды
сульфинила, ок-сидигалогениды серы(IV)], соед. общей ф-лы SOHal2,
где Hal = Cl, Вr, F (см. табл.).
Молекулы SOHal2
имеют пирамидальное строение. Для SOCl2 длины связей (нм) 0,207 (S-Cl),
0,145 (S—О), углы C1SC1 114°, OSCt 106°; для SOF2 длины связей
(нм) 0,159 (S—F), 0,14 (S—О), углы OSF 107°, FSF 93-96°. Термич. устойчивость
тионилгалогенидов резко уменьшается в ряду F > С1 > Вr; тионилфторид устойчив до ~ 500
°С; SOCl2 при нагр. выше т-ры кипения начинает разлагаться с
образованием S2Cl2, SO2, Cl2, а
при 440 °С наблюдается полный распад; тионил-бромид уже при комнатной т-ре
при длит. хранении разлагается на Вr2, SO2, S2Br2.
Все тионилгалогениды раств. в бензоле,
СНСl3, a SOBr2-также в CS2, ССl4.
Способность к гидролизу увеличивается в ряду F > > Сl > Вr; SOF2
гидролизуется медленно, давая HF и H2SO3; SOCl2
с холодной водой образует H2SO3 и НС1, с горячей-также
H2SO4 и S; SOBr2 легко гидролизуется, давая
H2SO3 и НВr. Тионилгалогениды реагируют с этанолом, р-рами щелочей.
Тионилфторид ниже 125°С практически не взаимод. с переходными металлами
(Mn, Fe, Co, Ni и др.); SOCl2 реагирует со мн. металлами при ~100°С
с образованием хлоридов, оксидов, сульфидов, SOBr2 вступает в аналогичные
р-ции при более низких т-рах, чем SOCl2. Тионилфторид начинает реагировать
со стеклом лишь при т-рах выше 480 °С.
Известны малоустойчивые
смешанные тионилгалогениды: SOFBr, а также SOFCl (бесцв. газ, т. пл. -139°С, т. кип. 12,2°С,
плотн. 1,580 г/см3 при 0°С).
В пром-сти тионилхлорид
получают взаимод. S, О2 и Сl2 при 180-200 °С в присут.
активного угля, его получают также р-цией избытка SO2 с ССl4
при 150°С и давлении ок. 4 МПа в присут. АlСl3. Тионилфторид
синтезируют действием HF на SOCl2, тионилбромид-взаимод. SOCl2
с НВr при 0°С.
Тионилхлорид применяют
для сульфохлорирования полимеров, как хлорирующий агент (напр., в произ-ве каучука,
красителей, лек. ср-в), как ускоритель полимеризации нек-рых
производных этилена. Тионилбромид-бромирующий агент в орг. синтезе.
Тионилгалогениды токсичны, поражают дыхат.
пути, слизистые оболочки, жидкие тионилгалогениды вызывают ожоги кожи. И. Н. Один.