ТИАМИН (витамин
Bt), водорастворимый витамин группы В. Существует в виде солей, важнейшая
из к-рых тиамин-гидрохлорид (ф-ла Ia, Х = Сl-·НС1; мол. м.
337,27); кристаллизуется с 1/2 H2О в виде бесцв. моноклинных
игл с т. пл. 240-244 и 250-252 °С (диаморфизм). Для водного р-ра тиамина при
рН 7,0 lмакс 233-235 и 265-267 нм, в кислой среде-245-247 нм.
Известны также тиаминбромид (Iа, X = Br- · НВr; т. пл.
220 и 229-231 °C) и тиаминмононитрат (Ia, X =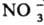 ·HN03;
т. пл. 164-165 и 196-200 °С). Соли тиамина хорошо
раств. в воде, хуже в спиртах, не раств. в эфире, хлороформе, бензоле и ацетоне.
·HN03;
т. пл. 164-165 и 196-200 °С). Соли тиамина хорошо
раств. в воде, хуже в спиртах, не раств. в эфире, хлороформе, бензоле и ацетоне.
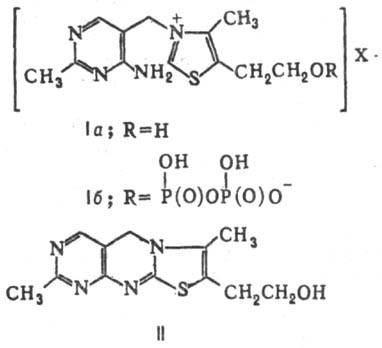
Тиамин устойчив в кислой среде
к нагреванию и действию окислителей, в щелочной среде легко окисляется в тиохром
(II)-желтое в-во с т. пл. 227°С (с разл.), обладающее в щелочной среде интенсивной
синей флуоресценцией с lмакс 460-470 нм.
Тиамин широко распространен
в живой природе. Синтезируется растениями и мн. микроорганизмами. Животные и
человек не синтезируют тиамин и должны получать его с пищей. Наиб. богаты тиамином (в
скобках приведено содержание тиамина в мг на 100 г продукта) дрожжи (0,6), хлеб и
хлебобулочные изделия из муки грубого помола или витаминизир. муки (ок. 0,3);
крупы-особенно гречневая (0,43), овсяная (0,49), пшенная (0,42); зернобобовые
(до 0,9); печень (0,3), нежирная свинина (0,52). Молоко и молочные продукты
так же, как и большинство овощей, бедны тиамином.
Тиамин присутствует в живых
организмах в форме свободного тиамина и его фосфорных эфиров: тиаминмонофосфата (ТМФ),
тиаминдифосфата (ТДФ; ф-ла Iб, X = НСl) и тиаминтри-фосфата (ТГФ).
Осн. формой, на долю к-рой в разл. органах и тканях человека приходится 60-80%
общего содержания тиамина, является ТДФ, синтезируемый в тканях из тиамина и АТФ при участии
фермента тиаминкиназы. ТДФ - кофермент важнейших ферментов углеводного обмена:
пируватдегидро-геназы, 2-оксоглутаратдегидрогеназы, дегидрогеназы кето-кислот
с разветвленной боковой цепью и транскетолазы.
ТДФ-зависимая пируватдегидрогеназа
принимает участие в окислит. декарбоксилировании пировиноградной к-ты (пирувата)
с образованием ацетилкофермента А. При этом пируват, образующийся в результате
гликолитич. расщепления глюкозы (см. Гликолиз), включается в трикарбоновых
кислот цикл, где окисляется до СО2 и Н2О. Общее кол-во
энергии, получаемой в результате окисления пирувата в этом цикле, почти в 4
раза превосходит энергию, освобождаемую в предшествующих р-циях гликолиза. Образующийся
в этом процессе ацетилкофермент А служит донором остатка уксусной к-ты ("активного
ацетата") для синтеза жирных к-т, стеринов, в т.ч. холестерина, стероидных
гормонов, желчных к-т, ацетилхолина и др.
Др. ТДФ-зависимый фермент-2-оксоглутаратдегидроге-наза,
катализирующая окислит. декарбоксилирование 2-оксоглутаровой к-ты с образованием
янтарной к-ты. Это превращение - важный этап цикла трикарбоновых к-т.
Кроме того, ТДФ принимает
участие в окислит. декарбо-ксилировании кетокислот с разветвленным углеродным
скелетом - 2-оксоизовалериановой, З-метил-2-оксовалериано-вой и 4-метил-2-оксопентановой,
являющихся продуктами дезаминирования аминокислот валина, изолейцина и лейцина.
Эти р-ции играют важную роль в катаболизме белков.
Транскетолаза, в
состав к-рой входит ТДФ,-один из ферментов пентозофосфатного цикла окисления
углеводов, являющегося осн. источником восстановленного никотин-амиддинуклеотидфосфата
(НАДФН) и рибозо-5-фосфата (первый используется как донор водорода в многочисл.
р-циях восстановления, второй входит в состав нуклеотидов и нуклеиновых к-т).
ТДФ, входя в состав активного
центра ферментов, принимает непосредств. участие в механизме ферментативного
катализа (см. Коферменты).
Потребность человека в
тиамине составляет. 0,5 мг на 1000 ккал (4186 кДж) суточного рациона или от 1,5 до
2,5 мг/сут в зависимости от энергозатрат.
Недостаток тиамина в организме
ведет к накоплению в крови и тканях недоокисленных продуктов обмена в-в, что,
в свою очередь, приводит к патофизиол. и патоморфологич. изменениям, создающим
картину В1-авитаминоза, одной из форм к-рого является болезнь бери-бери
(полиневрит, сердечно-сосудистые расстройства, отеки и др.).
Наиб. значит. патологич.
изменения при недостаточности тиамина развиваются в пищеварит., нервной и сердечно-сосудистой
системах. Характерным проявлением В1-авитаминоза является также общее
истощение организма, потеря веса.
Недостаток тиамина может возникнуть
при преимуществ. питании очищенным рисом, продуктами из муки высокого помола,
бедной тиамином. У пожилых людей недостаток тиамина, как и ряда др. витаминов, м. б. обусловлен
общим снижением кол-ва потребляемой пищи. Одна из важных причин недостатка тиамина-
нарушение всасывания витаминов при хронич. заболеваниях кишечника-хронич. энтеритах,
энтероколитах и т.п.
В пром-сти тиамин получают
конденсацией 4-амино-5-амино-метил-2-метилпиримидина, сероуглерода и 1-хлор-5-ацето-кси-2-пентанона
либо конденсацией 4-амино-5-галогено-2-метилпиримидина с 5-(2-гидроксиэтил)-4-метилтиазолом.
ТДФ получают взаимодействием тиамина с пирофосфорной к-той.
Тиамин применяют для профилактики
и лечения B1-гипо- и авитаминозов, при периферич. и алкогольных невритах,
энцефалопатии Вернике, сердечно-сосудистой недостаточности; ТДФ (кокарбоксилаза)-при
сахарном диабете, сердечно-сосудистых заболеваниях.
Лит.: Спиричев В.
Б.,в кн.: Молекулярные основы патологии, под ред. В. Н. Ореховича, М., 1966,
с. 220-68; Кокарбоксилаза и другие тиаминфосфаты, под ред. Ю. М. Островского,
Минск, 1974; Островский Ю.М., в кн.: Витамины, под ред. М.И. Смирнова, М., 1974,
с. 173-213; его же, Активные центры и группировки в молекуле тиамина, Минск,
1975; его же, в кн.: Экспериментальная витаминология, Минск, 1979, с. 176-223;
Спиричев В. Б., Ба-рашнев Ю. И., Врожденные нарушения обмена витаминов, М.,
1977.
В. Б. Спиричев.