ДИАМИНЫ, содержат в молекуле две аминогруппы. Наиб. значение имеют алифатич. a, w-диамины (С2-С12), моно- и бициклич. ароматич. и алициклич. первичные диамины, а также ряд вторичных и третичных диаминов. В природе наиб. известны пента- и тетраметилендиамины Н2N(СН2)nNН2, где п = 5 и 4, содержащиеся в продуктах гнилостного распада белков - соотв. кадаверин и путресцин (т. пл. 9 и 27-28 °С, т. кип. 178-179 и 159 °С; d425 0,873 и 0,877; легко раств. в воде и этаноле, плохо - в диэтиловом эфире). Образуются при ферментативном декарбоксилировании соотв. лизина и орнитина. Кадаверин найден в спорынье, мухоморе, сыре, пивных дрожжах. Путресцин - исходное соед. для синтеза физиологически активных полиаминов (спермидина и спермина). Большинство диаминов - бесцв. кристаллы; хорошо раств. в воде и спирте. Обладают всеми хим. св-вами, характерными для моноаминов (см. Амины). Сильные основания, образуют соли с к-тами. Диамины - двухкислотные основания; между первой и второй константами диссоциации различия могут достигать трех порядков, причем они резко уменьшаются для длинноцепных алифатич. a, w-диаминов (см. табл.).

Особенно высокой основностью (рКа 12,03) обладает 1,8-бис-(димстиламино)нафталин (т. наз. протонная губка). При повыш. т-рах диамины взаимод. с моно- и дикарбоновыми к-тами или их хлорангидридами, превращаясь в амидо-амины, диамиды или полиамиды. Последние образуются также при термич. дегидратации солей диаминов с карбоновыми к-тами. Эта р-ция лежит в основе пром. способа произ-ва ряда полиамидов (см., напр., Полигексаметиленадипинамид).
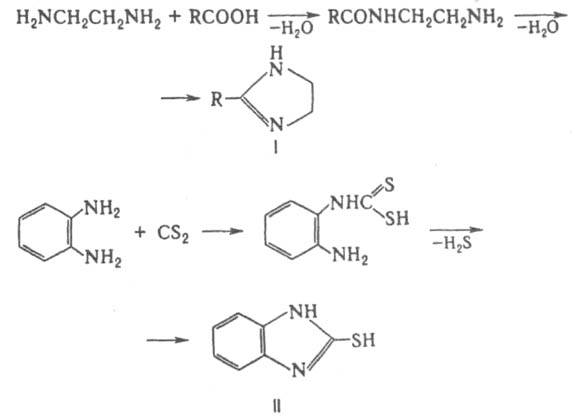
Алифатич. диамины в пром-сти получают: низшие - аммонолизом дигалогензамещенных углеводородов, напр.: СlСН2СН2Сl + 2NH3 : H2NCH2CH2NH2; восстановит. аминированием аминоспиртов либо акрилонитрила:
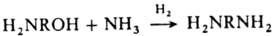 ; CH2=CHCN + NH3 + 2Н2 : H2NCH2CH2CH2NH2; высшие - обычно гидрированием динитрилов:
; CH2=CHCN + NH3 + 2Н2 : H2NCH2CH2CH2NH2; высшие - обычно гидрированием динитрилов: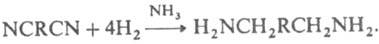
Алифатич. диамины могут быть получены также восстановит. аминированием дикарбоновых к-т и лактамов или гидрированием аминонитрилов. Препаративно алифатич. диамины синтезируют по р-циям Габриеля, Гофмана, Шмидта, гидроаминированием продуктов озонолиза циклоолефинов, аминированием гликолей и др. Нек-рые высшие диамины синтезируют на основе бутадиена и гидроксиламина:
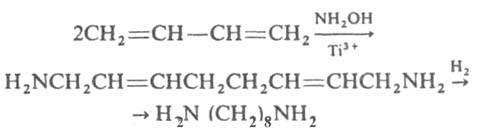
Ароматич. диамины в пром-сти чаще всего получают каталитич. гидрированием соответствующих динитросоединений или нитроанилинов, реже - восстановлением (Fe с НСl или H2SO4, Na2S) этих же соединений. Препаративно ароматич. диамины синтезируют по р-ции Гофмана, аминированием изомеров дихлорбензола или хлоранилина водным р-ром NH3 в присут. галогенидов Сu. Алициклич. диамины могут быть получены аналогично алифатич. диаминам. Шестичленные алициклич. диамины обычно синтезируют гидрированием ароматич. диаминов, динитросоединений или нитроанилинов, напр.:
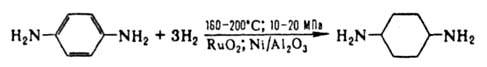
Они м. б. получены также перегруппировкой диамидов или диазидов циклогександикарбоновых к-т по Гофману и Курциусу соответственно. Третичные алифатич., ароматич. и алициклич. диамины синтезируют алкилированием соответствующих первичных диаминов алкилгалогенидами, спиртами, диметилсульфатом или восстановит аминированием альдегидов диаминами. Важнейшие циклич. диамины (пиперазин и его аналоги) в пром-ти обычно получают циклоаминированием моно- и диалканоламинов, а также циклизацией N-(b-гидроксиэтил)-этилендиамина, дезаминированием диэтилентриамина, пиролизом гидрохлоридов моноалканоламинов и др. Применяют диамины в произ-ве полиамидов, полиимидов, полимочевин, полиуретанов, ПАВ, ВВ, текстильно-вспомогат. в-в, красителей, ингибиторов коррозии и термич. полимеризации диеновых углеводородов, ионообменных смол, присадок, антиоксидантов и др. См., напр., Бензидин, Гексаметилендиамин, Диаминоантрахиноны, Диаминодиоксиантрахиноны, 4,4'-Диаминодифенилметан, 4,4'-Диаминодифениловый эфир, "Диамины", Додекаметилендиамин, Ксилилендиамины, Пиперазин, Толуилендиамины, Фенилендиамины, Этилендиамин.
===
Исп. литература для статьи «ДИАМИНЫ»: ТомиловА. П., Смирнов С. К., Адиподинитрил и гексаметилендиамин, М., 1974; Мономеры для поликонденсации. Сб. ст., пер. с англ., М., 1976; Якушкин М. И., Производство динитрилов фталевых кислот и ксилилен-диаминов, в кн. Справочник нефтехимика, т. 2, Л., 1978, с. 278; Общая органическая химия, пер. с англ., т. 3, М., 1982, с. 113-23; Kirk-Othmer encyclopedia, 3 cd., v.7, N.Y.. 1979. p. 580 96; v.2, N. Y., 1978. p. 348-54; Barnеs C.M., Rase H.F.. "Ind. Eng. Chem. Prod. Res. Dev.", 1981. v.20, № 2. p. 399-407. М. И. Якушкин.
Страница «ДИАМИНЫ» подготовлена по материалам химической энциклопедии.
Еще по теме:
Активные темы форума