6.8.5. Метод солюбилизации нерастворимого в воде красителя
Мицеллярная молекулярная масса может быть определена способом, специфическим только для мицеллярных растворов ПАВ - солюбилизации нерастворимого в воде красителя оранжевого ОТ. Этот метод был предложен Г. Шоттом. Метод основан на двух наблюдениях:
1) при концентрации раствора ниже ККМ краситель не солюбилизируется или солюбилизируется незначительно;
2) в растворах, насыщенных красителем оранжевым ОТ, только одна молекула красителя солюбилизируется мицеллой.
Экспериментальный процесс состоит из насыщения красителем водных растворов ПАВ известной концентрации, отделения избытка красителя и измерения поглощения света. Исходя из этих данных, определения коэффициента молярного погашения красителя и ККМ поверхностно-активного вещества, можно легко вычислить мицеллярную массу.
Такой метод экспериментально и теоретически менее сложен, чем метод рассеяния света, ультрацентрифугирования и др. Кроме того, нет необходимости определять или предполагать форму мицелл, присутствующих в растворе.
Согласно закона Ламберта-Беера
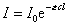 (2.6.45)
(2.6.45)
или
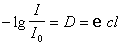 . (2.6.46)
. (2.6.46)
Определяя зависимость оптической плотности растворов с солюбилизированным красителем от концентрации растворенного ПАВ по величине dD/dc можно рассчитать мицеллярную массу.
Если известен коэффициент молярного погашения света раствором красителя, то
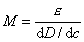 , (2.6.47)
, (2.6.47)
где с- концентрация поверхностно-активного вещества в г/л; l-длина кюветы в см; e -коэффициент молярного погашения света раствором красителя (л/моль·см); D- оптическая плотность при данной длине волны света. Значение dD/dcнаходится графическим путем.
Обозначая 1/ (dD/dc) через b, имеем
M=be l . (2.6.48)
Г. Шотт исследовал растворы ряда образцов ионогенных и неионогенных ПАВ методом солюбилизации красителя, светорассеяния и седиментации в поле ультрацентрифуги. Сравнение результатов измерений трех методов указало, что солюбилизированный краситель не оказывает влияния на степень агрегации мицелл неионогенных ПАВ.
Метод солюбилизации красителя имеет более высокую точность определения мицеллярных молекулярных масс, чем другие методы. Однако область его применения ограничена неионогенными веществами и не распространяется на растворы ионных ПАВ с длинным углеводородным радикалом. Для таких систем солюбилизационный предел может отклоняться от единицы. Было найдено, что мицеллярная масса некоторых ионогенных ПАВ, например, децилсульфата натрия, найденная по солюбилизации красителя, в несколько раз больше, чем представляется по данным рассеяния света. Несмотря на то, что значения мицеллярной молекулярной массы (МММ), найденные по светорассеянию, несомненно занижены, так как не было сделано коррекции на заряд мицелл, маловероятно, что поправка на заряд может значительно изменить величину MMМ. Возможны два источника ошибок при сравнении MMМ, найденных по светорассеянию и солюбилизации:
1) значительные отклонения найденных по светорассеянию величин от действительных как результат отклонения мицелл от сферичности и отсутствия поправок на заряд;
2) отклонения солюбилизационного предела от единицы.
Первый источник ошибок устраняется путем введения больших количеств нейтрального электролита, что подавляет диффузию противоионов, но наряду с этим изменяет также число агрегации мицелл. Кроме того, сoлюбилизaциoнный предел может зависеть от концентрации добавленного электролита.
В воде и разбавленных растворах электролитов краситель имеет очень малую растворимость (менее 2·10-9 моль/л), но умеренно переходит в раствор, содержащий большое количество электролита. Это может привести к изменению солюбилизационного предела.
Тем не менее, растворимость красителя в углеводородном ядре мицелл значительно выше, чем в водной среде, и поэтому наиболее вероятна локализация молекул красителя в мицеллах, без контакта с водной фазой. Можно предполагать, что молекулы красителя даже служат зародышами мицеллообразования. Естественно, что мицеллы находятся в динамическом равновесии, флуктуируя около некоторого среднего значения числа агрегации.
Когда мицелла, содержащая краситель, диссоциирует, возможно, несколько молекул ПАВ остаются в контакте с молекулой красителя и этот агрегат служит затем ядром для образования новой мицеллы. В случае большого количества зародышей в системе возможно некоторое занижение МММ. Однако, нельзя полностью исключить вероятность выхода молекул красителя из мицелл, так что часть их может оказаться пустыми. Если доля пустых мицелл будет достаточно велика, возможно некоторое завышение значений МММ. Трудно установить, какой из этих двух возможных случаев имеет на практике доминирующее значение.
В некоторых случаях и мицеллы неионогенных ПАВ способны поглотить более одной молекулы красителя. Такое явление наблюдалось, например, в растворах 18-оксиэтилированного октадецилового спирта, что связано с большим размером углеводородного ядра мицелл этого ПАВ, в котором могут разместиться несколько молекул красителя.
Таким образом, следует применять метод солюбилизации красителя с известной осторожностью, избегать использования его для растворов ионогенных веществ, а также неионогенных ПАВ, содержащих в углеводородном радикале более 16 атомов углерода.