Этилена окись, этиленоксид, оксиран,
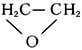 , простейший представитель эпоксидов (циклических простых эфиров с a-окисным трёхчленным кольцом), бесцветный газ с эфирным запахом; tпл — 111,3°С, tkип 10,7°С, плотность 0,891 г/см3 (4°С). Этилена окись хорошо растворима в воде, спирте, эфире и многих других органических растворителях; легко воспламеняется; образует с воздухом взрывоопасные смеси (3—80% по объёму). Химические свойства этилена окиси определяются наличием напряжённого и вследствие этого сравнительно легко размыкающегося (под действием высокой температуры и различных химических реагентов) эпоксидного цикла. Так, при нагревании до 400°С (в присутствии Al2O3 — при 150—300°С) этилена окись изомеризуется в ацетальдегид; гидрирование этилена окиси (над никелем при 80°С) приводит к этиловому спирту
, простейший представитель эпоксидов (циклических простых эфиров с a-окисным трёхчленным кольцом), бесцветный газ с эфирным запахом; tпл — 111,3°С, tkип 10,7°С, плотность 0,891 г/см3 (4°С). Этилена окись хорошо растворима в воде, спирте, эфире и многих других органических растворителях; легко воспламеняется; образует с воздухом взрывоопасные смеси (3—80% по объёму). Химические свойства этилена окиси определяются наличием напряжённого и вследствие этого сравнительно легко размыкающегося (под действием высокой температуры и различных химических реагентов) эпоксидного цикла. Так, при нагревании до 400°С (в присутствии Al2O3 — при 150—300°С) этилена окись изомеризуется в ацетальдегид; гидрирование этилена окиси (над никелем при 80°С) приводит к этиловому спирту

гидрогалогенирование — к соответствующим этиленгалогенгидринам (например,

В этих и многих аналогичных реакциях этилена окись является эффективным алкилирующим агентом (с её помощью вводится b-оксиэтильная группа HOCH2CH2—), что широко используется в промышленности и лабораторной практике для получения ценных продуктов, например этиленциангидрина (взаимодействием с синильной кислотой), этиленгликоля и его моноэфиров — целлозольвов (гидратацией и алкоголизом), этаноламинов (реакцией с аммиаком), b-меркаптоэтанола HSC2CH2OH и (взаимодействием с сероводородом), b-фенил-этилового спирта (Фриделя — Крафтса реакцией с бензолом). Для этилена окиси характерна (также идущая с разрывом связи С—О) полимеризация. Так, при пропускании паров этилена окиси при 110—160°С над NaHSO4 образуется её димер — диоксан; под каталитическим действием третичных аминов или хлорида олова (IV) этилена окись легко полимеризуется (иногда со взрывом) уже при обычной температуре. Полиэтиленоксиды [—CH2—CH2—O] n имеют широкий интервал молекулярных масс (от 102 до 107). Различают низкомолекулярные полимеры, т. н. полиэтиленгликоли (молекулярная масса до 40 тыс.), и высокомолекулярные (от 500 тыс. до 10 млн.). Полиэтиленгликоли — жидкие или воскообразные продукты, получаемые каталитической полимеризацией этилена окиси при 100 — 150°С и используемые в текстильной промышленности (как смачиватели, умягчители и антистатические агенты), в косметике и как компоненты моющих средств. Высокомолекулярные полимеры этилена окиси в промышленности получают суспензионной каталитической полимеризацией при 20—50°С; они представляют собой твёрдые продукты с хорошими термопластическими и механическими свойствами, некоторой водорастворимостью; используются как флокулянты, для снижения гидродинамического сопротивления водных потоков, в текстильной промышленности (как загустители). В качестве эмульгаторов и компонентов моющих средств применяются продукты конденсации этилена окиси с высшими спиртами (олеиловым, лауриловым, стеариловым), алкилфенолами, например с изооктилфенолом, с жирными карбоновыми кислотами, представляющие собой полиэтиленгликолевые эфиры типа RO (CH2CH2O)n—Н, где R — органический радикал, а
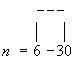 .
.
Циклические простые эфиры, получаемые из этилена окиси, — т. н. краунэфиры, широко применяют в органическом синтезе для разъединения ионных пар различных солей в апротонных биполярных растворителях, как, например, краун 18—6 для связывания иона калия. Основные промышленные методы получения этилена окиси — каталитическое окисление этилена кислородом воздуха при 200—300°С над катализатором, содержащим металлическое серебро, и дегидрохлорирование этиленхлоргидрина. Важное значение этилена окись имеет также в тонком органическом синтезе: например реакцией её с ацетоуксусным эфиром получают ацетобутиролактон, используемый в производстве витамина B1 и являющийся промежуточным продуктом для получения противомалярийных препаратов. Этилена окись токсична: в малых количествах она обладает наркотическим действием, в значительных — приводит к раздражению слизистых оболочек, удушью и отёку лёгких. Предельно допустимая концентрация этилена окиси в воздухе — 0,001 мг/л.