Хлорирование органических соединений, процесс прямого замещения в органических соединениях атомов водорода атомами хлора. Хлорирование может быть осуществлено действием свободного хлора или веществами, его генерирующими, например хлористым сульфурилом SO2Cl2 (см. Сульфурила галогениды). Механизм хлорирования определяется природой органического соединения и условиями реакции. Так, насыщенные углеводороды взаимодействуют с хлором при облучении ультрафиолетовым светом (УФ-облучении) по радикально-цепному механизму:
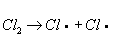 ;
; 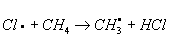 ;
;
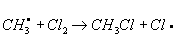 и т. д.
и т. д.
Эта реакция лежит в основе промышленного способа получения из метана метилхлорида, метиленхдорида, хлороформа, четырёххлористого углерода, из пентановых фракций бензина — амилхлоридов. Хлорирование органических соединений ароматического ряда протекает по ионному механизму в присутствии кислотного катализатора, например AlCl3 или FeCl3. Т. о. в промышленности получают, например, хлорбензол:
Cl2 + FeCl3 ® С+ + [FeCl4]-;
C6H6 + Cl+ ® C6H5Cl + Н+;
[FeCl4]- + H+ ® FeCl3 + HCl.
Принимая во внимание различия в механизмах хлорирования органических соединений алифатических и ароматических рядов, регулируют хлорирование жирно-ароматических углеводородов: прибавление FeCl3 ведёт к замещению атомов водорода в ароматическом ядре, тогда как УФ-облучение и повышение температуры способствуют хлорированию боковых алифатических групп. Так, в промышленности хлорированием толуола получают хлортолуолы (в присутствии FeCl3) или бензилхлорид C6H5CH2Cl (под действием УФ-облучения). При высокой температуре удаётся осуществить прямое замещение атомов водорода на хлор и в алкильных группах олефинов (с сохранением кратной связи), например:
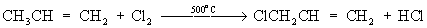
Эта реакция используется в промышленности для получения аллилхлорида — исходного продукта в производстве глицерина.
Иногда под хлорированием в более широком смысле понимают создание связи С—Cl любым способом, например присоединением по кратным связям хлора, хлористого водорода, хлорноватистой кислоты, хлористого нитрозила, замещением на хлор др. функциональных групп (гидроксильной в спиртах и карбоновых в кислотах, аминогруппы в ароматических аминах после предварительного их диазотирования и др.). Так, в промышленности присоединением хлора к этилену получают дихлорэтан, являющийся сырьём в одном из способов производства винилхлорида; хлорированием ацетилена — тетрахлорэтан, применяемый для получения трихлорэтилена, хлорированием некоторых каучуков — хлор-каучуки. Реакцией ненасыщенных соединений с хлористым водородом в промышленности производят винилхлорид, этилхлорид, хлоропрен. Хлорирование используется также для получения инсектицидов (гексахлорана, полихлорпинена, полихлоркамфена), гербицидов, например эфиров 2,4-дихлор-феноксиуксусной кислоты, гексахлорэтана (заменителя камфары) и др. важных продуктов.