Тритий (лат. Tritium), Т (или 3H), радиоактивный изотоп водорода с массовым числом 3 (отсюда название: от греч. trítos — третий). Открыт в 1934 английским учёными Э. Резерфордом, М. Л. Олифантом и П. Хартеком. Ядро трития состоит из одного протона и двух нейтронов. Тритий b-активен; период полураспада T1/2 = 12,26 года. В природе образуется в незначительных количествах под действием нейтронов космических лучей на атомы азота  и при ядерных превращениях под действием космических частиц высоких энергий. Среднее содержание трития в природных водах 1 атом на 1018 атомов 1H. Получают тритий в ядерных реакторах, облучая нейтронами
и при ядерных превращениях под действием космических частиц высоких энергий. Среднее содержание трития в природных водах 1 атом на 1018 атомов 1H. Получают тритий в ядерных реакторах, облучая нейтронами
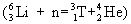 . Тритий применяется как важнейший компонент в реакциях термоядерного синтеза, как горючее в термоядерных бомбах, а также в химических, биологических и гидрологических исследованиях (см. Изотопные индикаторы).
. Тритий применяется как важнейший компонент в реакциях термоядерного синтеза, как горючее в термоядерных бомбах, а также в химических, биологических и гидрологических исследованиях (см. Изотопные индикаторы).
Лит.: Эванс Э., Тритий и его соединения, пер. с англ., М., 1970.