Титан (лат. Titanium), Ti, химический элемент IV группы периодической системы Менделеева; атомный номер 22, атомная масса 47,90; имеет серебристо-белый цвет, относится к лёгким металлам. Природный титан состоит из смеси пяти стабильных изотопов: 46Ti (7,95%), 47Ti (7,75%), 48Ti (73,45%), 49Ti (5,51%), 50Ti (5,34%). Известны искусственные радиоактивные изотопы 45Ti (Ti1/2 = 3,09ч, 51Ti (Ti1/2 = 5,79 мин) и др.
Историческая справка. Титан в виде двуокиси был открыт английским любителем-минералогом У. Грегором в 1791 в магнитных железистых песках местечка Менакан (Англия); в 1795 немецкий химик М. Г. Клапрот установил, что минерал рутил представляет собой природный окисел этого же металла, названного им «титаном» [в греческой мифологии титаны — дети Урана (Неба) и Геи (Земли)]. Выделить титан в чистом виде долго не удавалось; лишь в 1910 американский учёный М. А. Хантер получил металлический титан нагреванием его хлорида с натрием в герметичной стальной бомбе; полученный им металл был пластичен только при повышенных температурах и хрупок при комнатной из-за высокого содержания примесей. Возможность изучать свойства чистого титана появилась только в 1925, когда нидерландские учёные А. Ван-Аркел и И. де Бур методом термической диссоциации иодида титана получили металл высокой чистоты, пластичный при низких температурах.
Распространение в природе. Титан — один из распространённых элементов, среднее содержание его в земной коре (кларк) составляет 0,57% по массе (среди конструкционных металлов по распространённости занимает 4-е место, уступая железу, алюминию и магнию). Больше всего титана в основных породах так называемой «базальтовой оболочки» (0,9%), меньше в породах «гранитной оболочки» (0,23%) и ещё меньше в ультраосновных породах (0,03%) и др. К горным породам, обогащенным титаном, относятся пегматиты основных пород, щелочные породы, сиениты и связанные с ними пегматиты и др. Известно 67 минералов титана, в основном магматического происхождения; важнейшие — рутил и ильменит (см. также Титановые руды).
В биосфере титан в основном рассеян. В морской воде его содержится 1·10-7%; титан — слабый мигрант.
Физические свойства. Титан существует в виде двух аллотропических модификаций: ниже температуры 882,5 °С устойчива a-форма с гексагональной плотноупакованной решёткой (а = 2,951 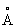 , с = 4,679
, с = 4,679 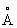 ), а выше этой температуры — b-форма с кубической объёмно-центрированной решёткой а = 3,269
), а выше этой температуры — b-форма с кубической объёмно-центрированной решёткой а = 3,269 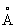 . Примеси и легирующие добавки могут существенно изменять температуру a/b превращения.
. Примеси и легирующие добавки могут существенно изменять температуру a/b превращения.
Плотность a-формы при 20 °С 4,505 г/см3 а при 870 °С 4,35 г/см3 b-формы при 900 °С 4,32 г/см3; атомный радиус Ti 1,46 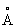 , ионные радиусы Ti+ 0,94
, ионные радиусы Ti+ 0,94 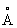 , Ti2+ 0,78
, Ti2+ 0,78 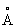 , Ti3+ 0,69
, Ti3+ 0,69 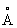 , Ti4+ 0,64
, Ti4+ 0,64 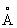 , tпл1668±5°С, tкип 3227 °С; теплопроводность в интервале 20—25 °С 22,065 вт/(м × К) [0,0527 кал/(см × сек × °С)]; температурный коэффициент линейного расширения при 20 °С 8,5×10-6, в интервале 20—700 °С 9,7×10-6; теплоёмкость 0,523 кдж/(кг × К) [0,1248 кал/(г ×°С)]; удельное электросопротивление 42,1×10-6 ом ×см при 20 °С; температурный коэффициент электросопротивления 0,0035 при 20 °С; обладает сверхпроводимостью ниже 0,38±0,01 К. Титан парамагнитен, удельная магнитная восприимчивость (3,2±0,4)×10-6 при 20°С. Предел прочности 256 Мн/м2 (25,6 кгс/мм2), относительное удлинение 72%, твёрдость по Бринеллю менее 1000 Мн/м2 (100 кгс/мм2). Модуль нормальной упругости 108000 Мн/м2 (10800 кгс/мм2). Металл высокой степени чистоты ковок при обычной температуре.
, tпл1668±5°С, tкип 3227 °С; теплопроводность в интервале 20—25 °С 22,065 вт/(м × К) [0,0527 кал/(см × сек × °С)]; температурный коэффициент линейного расширения при 20 °С 8,5×10-6, в интервале 20—700 °С 9,7×10-6; теплоёмкость 0,523 кдж/(кг × К) [0,1248 кал/(г ×°С)]; удельное электросопротивление 42,1×10-6 ом ×см при 20 °С; температурный коэффициент электросопротивления 0,0035 при 20 °С; обладает сверхпроводимостью ниже 0,38±0,01 К. Титан парамагнитен, удельная магнитная восприимчивость (3,2±0,4)×10-6 при 20°С. Предел прочности 256 Мн/м2 (25,6 кгс/мм2), относительное удлинение 72%, твёрдость по Бринеллю менее 1000 Мн/м2 (100 кгс/мм2). Модуль нормальной упругости 108000 Мн/м2 (10800 кгс/мм2). Металл высокой степени чистоты ковок при обычной температуре.
Применяемый в промышленности технический титан содержит примеси кислорода, азота, железа, кремния и углерода, повышающие его прочность, снижающие пластичность и влияющие на температуру полиморфного превращения, которое происходит в интервале 865—920 °С. Для технического титана марок ВТ1-00 и ВТ1-0 плотность около 4,32 г/см3, предел прочности 300— 550 Мн/м2 (30—55 кгс/мм2), относительное удлинение не ниже 25%, твёрдость по Бринеллю 1150—1650 Мн/м2 (115—165 кгс/мм2). Конфигурация внешней электронной оболочки атома Ti 3d24s2.
Химические свойства. Чистый титан — химически активный переходный элемент, в соединениях имеет степени окисления + 4, реже +3 и +2. При обычной температуре и вплоть до 500—550 °С коррозионно устойчив, что объясняется наличием на его поверхности тонкой, но прочной окисной плёнки.
С кислородом воздуха заметно взаимодействует при температуре выше 600 °С с образованием TiO2 (см. также Титана окислы). Тонкая титановая стружка при недостаточной смазке может загораться в процессе механической обработки. При достаточной концентрации кислорода в окружающей среде и повреждении окисной плёнки путём удара или трения возможно загорание металла при комнатной температуре и в сравнительно крупных кусках.
Окисная плёнка не защищает титан в жидком состоянии от дальнейшего взаимодействия с кислородом (в отличие, например, от алюминия), и поэтому его плавка и сварка должны проводиться в вакууме, в атмосфере нейтрального газа или под флюсом. Титан обладает способностью поглощать атмосферные газы и водород, образуя хрупкие сплавы, непригодные для практического использования; при наличии активированной поверхности поглощение водорода происходит уже при комнатной температуре с небольшой скоростью, которая значительно возрастает при 400 °С и выше. Растворимость водорода в титане является обратимой, и этот газ можно удалить почти полностью отжигом в вакууме. С азотом титан реагирует при температуре выше 700 °С, причём получаются нитриды типа TiN; в виде тонкого порошка или проволоки титан может гореть в атмосфере азота. Скорость диффузии азота и кислорода в титане значительно ниже, чем водорода. Получаемый в результате взаимодействия с этими газами слой отличается повышенными твёрдостью и хрупкостью и должен удаляться с поверхности титановых изделий путём травления или механической обработки. Титан энергично взаимодействует с сухими галогенами (см. Титана галогениды), по отношению к влажным галогенам устойчив, так как влага играет роль ингибитора.
Металл устойчив в азотной кислоте всех концентраций (за исключением красной дымящейся, вызывающей коррозионное растрескивание титана, причём реакция иногда идёт со взрывом), в слабых растворах серной кислоты (до 5% по массе). Соляная, плавиковая, концентрированная серная, а также горячие органические кислоты: щавелевая, муравьиная и трихлоруксусная реагируют с титаном.
Титан коррозионно устойчив в атмосферном воздухе, морской воде и морской атмосфере, во влажном хлоре, хлорной воде, горячих и холодных растворах хлоридов, в различных технологических растворах и реагентах, применяемых в химической, нефтяной, бумагоделательной и др. отраслях промышленности, а также в гидрометаллургии. Титан образует с С, В, Se, Si металлоподобные соединения, отличающиеся тугоплавкостью и высокой твёрдостью. Карбид TiG (tпл 3140 °С) получают нагреванием смеси TiO2 с сажей при 1900—2000 °С в атмосфере водорода; нитрид TiN (tпл 2950 °С) — нагреванием порошка титана в азоте при температуре выше 700 °С. Известны силициды TiSi2, Ti5Si3, TiSi и бориды TiB, Ti2B5, TiB2. При температурах 400—600 °С титан поглощает водород с образованием твёрдых растворов и гидридов (TiH, TiH2). При сплавлении TiO2 со щелочами образуются соли титановых кислот мета- и ортотитанаты (например, Na2TiO3 и Na4TiO4), а также полититанаты (например, Na2Ti2O5 и Na2Ti3O7). К титанатам относятся важнейшие минералы титана, например ильменит FeTiO3, перовскит CaTiO3. Все титанаты малорастворимы в воде. Двуокись титана, титановые кислоты (осадки), а также титанаты растворяются в серной кислоте с образованием растворов, содержащих титанилсульфат TiOSO4. При разбавлении и нагревании растворов в результате гидролиза осаждается H2TiO3, из которой получают двуокись титана. При добавлении перекиси водорода в кислые растворы, содержащие соединения Ti (IV), образуются перекисные (надтитановые) кислоты состава H4TiO5 и H4TiO8 и соответствующие им соли; эти соединения окрашены в жёлтый или оранжево-красный цвет (в зависимости от концентрации титана), что используется для аналитического определения титана.
Получение. Наиболее распространённым методом получения металлического титана является магниетермический метод, то есть восстановление тетрахлорида титана металлическим магнием (реже — натрием):
TiCl4 + 2Mg = Ti + 2MgCl2.
В обоих случаях исходным сырьём служат окисные руды титана — рутил, ильменит и др. В случае руд типа ильменитов титан в форме шлака отделяется от железа путём плавки в электропечах. Шлак (так же, как рутил) подвергают хлорированию в присутствии углерода с образованием тетрахлорида титана, который после очистки поступает в восстановительный реактор с нейтральной атмосферой.
Титан по этому процессу получается в губчатом виде и после измельчения переплавляется в вакуумных дуговых печах на слитки с введением легирующих добавок, если требуется получить сплав. Магниетермический метод позволяет создать крупное промышленное производство титана с замкнутым технологическим циклом, так как образующийся при восстановлении побочный продукт — хлорид магния направляется на электролиз для получения магния и хлора.
В ряде случаев для производства изделий из титана и его сплавов выгодно применять методы порошковой металлургии. Для получения особо тонких порошков (например, для радиоэлектроники) можно использовать восстановление двуокиси титана гидридом кальция.
Мировое производство металлического титана развивалось весьма быстро: около 2 т в 1948, 2100 т в 1953, 20 000 т в 1957; в 1975 оно превысило 50 000 т.
Применение. Основные преимущества титана перед др. конструкционными металлами: сочетание лёгкости, прочности и коррозионной стойкости. Титановые сплавы по абсолютной, а тем более по удельной прочности (то есть прочности, отнесённой к плотности) превосходят большинство сплавов на основе др. металлов (например, железа или никеля) при температурах от -250 до 550 °С, а по коррозионности они сравнимы со сплавами благородных металлов (см. также Лёгкие сплавы). Однако как самостоятельный конструкционный материал титан стал применяться только в 50-е гг. 20 в. в связи с большими техническими трудностями его извлечения из руд и переработки (именно поэтому титан условно относили к редким металлам). Основная часть титана расходуется на нужды авиационной и ракетной техники и морского судостроения (см. также Титановые сплавы). Сплавы титана с железом, известные под названием «ферротитан» (20—50% титана), в металлургии качественных сталей и специальных сплавов служат легирующей добавкой и раскислителем.
Технический титан идёт на изготовление ёмкостей, химических реакторов, трубопроводов, арматуры, насосов и др. изделий, работающих в агрессивных средах, например в химическом машиностроении. В гидрометаллургии цветных металлов применяется аппаратура из титана. Он служит для покрытия изделий из стали (см. Титанирование). Использование титана даёт во многих случаях большой технико-экономический эффект не только благодаря повышению срока службы оборудования, но и возможности интенсификации процессов (как, например, в гидрометаллургии никеля). Биологическая безвредность титана делает его превосходным материалом для изготовления оборудования для пищевой промышленности и в восстановительной хирургии. В условиях глубокого холода прочность титана повышается при сохранении хорошей пластичности, что позволяет применять его как конструкционный материал для криогенной техники. Титан хорошо поддаётся полировке, цветному анодированию и др. методам отделки поверхности и поэтому идёт на изготовление различных художественных изделий, в том числе и монументальной скульптуры. Примером может служить памятник в Москве, сооруженный в честь запуска первого искусственного спутника Земли. Из соединений титана практического значение имеют окислы титана, галогениды титана, а также силициды титана, используемые в технике высоких температур; бориды титана и их сплавы, применяемые в качестве замедлителей в ядерных энергетических установках благодаря их тугоплавкости и большому сечению захвата нейтронов. Карбид титана, обладающий высокой твёрдостью, входит в состав инструментальных твёрдых сплавов, используемых для изготовления режущих инструментов и в качестве абразивного материала.
Двуокись титана и титанат бария служат основой титановой керамики, а титанат бария — важнейший сегнетоэлектрик.
С. Г. Глазунов.
Титан в организме. Титан постоянно присутствует в тканях растений и животных. В наземных растениях его концентрация — около 10-4%, в морских — от 1,2 ×10-3 до 8 ×10-2%, в тканях наземных животных — менее 2 ×10-4%, морских — от 2 ×10-4 до 2 ×10-2%. Накапливается у позвоночных животных преимущественно в роговых образованиях, селезёнке, надпочечниках, щитовидной железе, плаценте; плохо всасывается из желудочно-кишечного тракта. У человека суточное поступление титана с продуктами питания и водой составляет 0,85 мг; выводится с мочой и калом (0,33 и 0,52 мг соответственно). Относительно малотоксичен.
Лит.: Глазунов С. Г., Моисеев В. Н., Конструкционные титановые сплавы, М., 1974; Металлургия титана, М., 1968; Горощенко Я. Г., Химия титана, [ч. 1—2], К., 1970—72; Zwicker U., Titan und Titanlegierungen, B., 1974; Bowen H. I. M., Trace elements in biochemistry, L.— N. Y., 1966.