Сера (лат. Sulfur) S, химический элемент VI группы периодической системы Менделеева; атомный номер 16, атомная масса 32,06. Природная сера состоит из четырёх стабильных изотопов: 32S (95,02%), 33S (0,75%), 34S (4,21%), 36S (0,02%). Получены также искусственные радиоактивные изотопы 31S (T1/2 = 2,4 сек), 35S (T1/2 = 87,1 cym), 37S (T1/2 = 5,04 мин).
Историческая справка. Сера в самородном состоянии, а также в виде сернистых соединений известна с древнейших времён. Она упоминается в Библии, поэмах Гомера и др. Сера входила в состав «священных» курений при религиозных обрядах; считалось, что запах горящей серы отгоняет злых духов. Сера давно стала необходимым компонентом зажигательных смесей для военных целей, например «греческого огня» (10 в. н. э.). Около 8 в. в Китае стали использовать серу в пиротехнических целях. Издавна серой и её соединениями лечили кожные заболевания. В период арабской алхимии возникла гипотеза, согласно которой серу (начало горючести) и ртуть (начало металличности) считали составными частями всех металлов. Элементарную природу серы установил А. Л. Лавуазье и включил её в список неметаллических простых тел (1789). В 1822 Э. Мичерлих обнаружил аллотропию серы.
Распространение в природе. Сера относится к весьма распространённым химическим элементам (кларк 4,7·10-2); встречается в свободном состоянии (сера самородная) и в виде соединений — сульфидов, полисульфидов, сульфатов (см. Сульфиды природные, Сульфаты природные, Сульфидные руды). Вода морей и океанов содержит сульфаты натрия, магния, кальция. Известно более 200 минералов серы, образующихся при эндогенных процессах. В биосфере образуется свыше 150 минералов серы (преимущественно сульфатов); широко распространены процессы окисления сульфидов до сульфатов, которые в свою очередь восстанавливаются до вторичного H2S и сульфидов. Эти реакции происходят при участии микроорганизмов. Многие процессы биосферы приводят к концентрации серы — она накапливается в гумусе почв, углях, нефти, морях и океанах (8,9·10-2%), подземных водах, в озёрах и солончаках. В глинах и сланцах серы в 6 раз больше, чем в земной коре в целом, в гипсе — в 200 раз, в подземных сульфатных водах — в десятки раз. В биосфере происходит круговорот серы: она приносится на материки с атмосферными осадками и возвращается в океан со стоком. Источником серы в геологическом прошлом Земли служили главным образом продукты извержения вулканов, содержащие SO2 и H2S. Хозяйственная деятельность человека ускорила миграцию серы; интенсифицировалось окисление сульфидов.
Физические и химические свойства. Сера — твёрдое кристаллическое вещество, устойчивое в виде двух аллотропических модификаций. Ромбическая a-S лимонно-жёлтого цвета, плотность 2,07 г/см3, tпл 112,8 °С, устойчива ниже 95,6°С; моноклинная b-S медово-жёлтого цвета, плотность 1,96 г/см3, tпл 119,3 °С, устойчива между 95,6 °С и температурой плавления. Обе эти формы образованы восьмичленными циклическими молекулами S8 с энергией связи S — S 225,7 кдж/моль.
При плавлении сера превращается в подвижную жёлтую жидкость, которая выше 160 °С буреет, а около 190 °С становится вязкой тёмно-коричневой массой. Выше 190°С вязкость уменьшается, а при 300 °С сера вновь становится жидкотекучей. Это обусловлено изменением строения молекул: при 160 °С кольца S8 начинают разрываться, переходя в открытые цепи; дальнейшее нагревание выше 190 °С уменьшает среднюю длину таких цепей.
Если расплавленную серу, нагретую до 250—300 °С, влить тонкой струей в холодную воду, то получается коричнево-жёлтая упругая масса (пластическая сера). Она лишь частично растворяется в сероуглероде, в осадке остаётся рыхлый порошок. Растворимая в CS2 модификация называется l-S, а нерастворимая — m-S. При комнатной температуре обе эти модификации превращаются в устойчивую хрупкую a-S. tkип серы 444,6 °С (одна из стандартных точек международной температурной шкалы). В парах при температуре кипения, кроме молекул S8, существуют также S6, S4 и S2. При дальнейшем нагревании крупные молекулы распадаются, и при 900°С остаются лишь S2, которые приблизительно при 1500°С заметно диссоциируют на атомы. При замораживании жидким азотом сильно нагретых паров серы получается устойчивая ниже — 80°С пурпурная модификация, образованная молекулами S2.
Сера — плохой проводник тепла и электричества. В воде она практически нерастворима, хорошо растворяется в безводном аммиаке, сероуглероде и в ряде органических растворителей (фенол, бензол, дихлорэтан и др.).
Конфигурация внешних электронов атома S 3s23p 4. В соединениях сера проявляет степени окисления -2, +4, +6.
Сера химически активна и особенно легко при нагревании соединяется почти со всеми элементами, за исключением N2, I2, Au, Pt и инертных газов. СO2 на воздухе выше 300 °С образует окислы: SO2 — сернистый ангидрид и SO3 — серный ангидрид, из которых получают соответственно сернистую кислоту и серную кислоту, а также их соли сульфиты и сульфаты (см. также Тиокислоты и Тиосульфаты). Уже на холоду S энергично соединяется с F2, при нагревании реагирует с Cl2 (см. Серы фториды, Серы хлориды); с бромом сера образует только S2Br2, иодиды серы неустойчивы. При нагревании (150 — 200 °С) наступает обратимая реакция с H2 с получением сернистого водорода. Сера образует также многосернистые водороды общей формулы H2Sx, т. н. сульфаны. Известны многочисленные сераорганические соединения.
При нагревании сера взаимодействует с металлами, образуя соответствующие сернистые соединения (сульфиды) и многосернистые металлы (полисульфиды). При температуре 800—900 °С пары серы реагируют с углеродом, образуя сероуглерод CS2. Соединения серы с азотом (N4S4 и N2S5) могут быть получены только косвенным путём.
Получение. Элементарную серу получают из серы самородной, а также окислением сернистого водорода и восстановлением сернистого ангидрида. О способах добычи серы см. Серные руды. Источник сернистого водорода для производства серы — коксовые, природные газы, газы крекинга нефти. Разработаны многочисленные методы переработки H2S; наибольшее значение имеют следующие: 1) H2S извлекают из газов раствором моногидротиоарсената натрия:
Na2HAsS2 + H2S = Na2HAsS3O + H2O.
Затем продувкой воздуха через раствор осаждают серу в свободном виде:
NaHAsS3O + 1/2 O2 = Na2HAsS2O2 + S.
2) H2S выделяют из газов в концентрированном виде. Затем его основная масса окисляется кислородом воздуха до серы и частично до SO2. После охлаждения H2S и образовавшиеся газы (SO2, N2, CO2) поступают в два последовательных конвертора, где в присутствии катализатора (активированный боксит или специально изготовляемый алюмогель) происходит реакция:
2H2S + SO2 = 3S + 2H2O.
В основе получения серы из SO2 лежит реакция восстановления его углём или природными углеводородными газами. Иногда это производство сочетается с переработкой пиритных руд.
В 1972 элементарной серы в мире (без социалистических стран) произведено 32,0 млн. т; основная масса её добывалась из природных самородных руд. В 70-е гг. 20 в. первостепенное значение (в связи с открытием крупных месторождений сероводородсодержащих топливных газов) приобретают методы получения серы из H2S.
Сорта серы. Выплавленная непосредственно из серных руд сера называется природной комовой; полученная из H2S и SO2 — газовой комовой. Природная комовая сера, очищенная перегонкой, называется рафинированной. Сконденсированная из паров при температуре выше точки плавления в жидком состоянии и затем разлитая в формы — черенковой серой. При конденсации серы ниже точки плавления на стенках конденсационных камер образуется мелкий порошок серы — серный цвет. Особо высокодисперсная сера носит название коллоидной.
Применение. Сера применяется в первую очередь для получения серной кислоты: в бумажной промышленности (для получения сульфитцеллюлозы); в сельском хозяйстве (для борьбы с болезнями растений, главным образом винограда и хлопчатника); в резиновой промышленности (вулканизующий агент); в производстве красителей и светящихся составов; для получения чёрного (охотничьего) пороха; в производстве спичек.
И. К. Малина.
В медицинской практике применение серы основано на её способности при взаимодействии с органическими веществами организма образовывать сульфиды и пентатионовую кислоту, от присутствия которых зависят кератолитические (растворяющие — от греч. kéras — рог и lytikós — растворяющий), противомикробные и противопаразитарные эффекты. Сера входит в состав Вилькинсона мази и других препаратов, применяемых для лечения чесотки. Очищенную и осажденную серу употребляют в мазях и присыпках для лечения некоторых кожных заболеваний (себорея, псориаз и др.); в порошке — при глистных инвазиях (энтеробиоз); в растворах — для пиротерапии прогрессивного паралича и др.
Сера в организме. В виде органических и неорганических соединений сера постоянно присутствует во всех живых организмах и является важным биогенным элементом. Её среднее содержание в расчёте на сухое вещество составляет: в морских растениях около 1,2%, наземных — 0,3%, в морских животных 0,5—2%, наземных — 0,5%. Биологическая роль серы определяется тем, что она входит в состав широко распространённых в живой природе соединений: аминокислот (метионин, цистеин), и следовательно белков и пептидов; коферментов (кофермент А, липоевая кислота), витаминов (биотин, тиамин), глутатиона и другие Сульфгидрильные группы (— SH) остатков цистеина играют важную роль в структуре и каталитическая активности многих ферментов. Образуя дисульфидные связи (— S — S —) внутри отдельных полипептидных цепей и между ними, эти группы участвуют в поддержании пространственной структуры молекул белков. У животных сера обнаружена также в виде органических сульфатов и сульфокислот — хондроитинсерной кислоты (в хрящах и костях), таурохолиевой кислоты (в жёлчи), гепарина, таурина. В некоторых железосодержащих белках (например, ферродоксинах) сера обнаружена в форме кислотолабильного сульфида. Сера способна к образованию богатых энергией связей в макроэргических соединениях.
Неорганические соединения серы в организмах высших животных обнаружены в небольших количествах, главным образом в виде сульфатов (в крови, моче), а также роданидов (в слюне, желудочном соке, молоке, моче). Морские организмы богаче неорганическими соединениями серы, чем пресноводные и наземные. Для растений и многих микроорганизмов сульфат (SO42-) наряду с фосфатом и нитратом служит важнейшим источником минерального питания. Перед включением в органические соединения сера претерпевает изменения в валентности и превращается затем в органическую форму в своём наименее окисленном состоянии; т. о. сера широко участвует в окислительно-восстановительных реакциях в клетках. В клетках сульфаты, взаимодействуя с аденозинтрифосфатом (АТФ), превращаются в активную форму — аденилилсульфат:
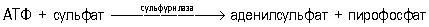
Катализирующий эту реакцию фермент — сульфурилаза (АТФ: сульфат — адснилилтрансфераза) широко распространён в природе. В такой активированной форме сульфонильная группа подвергается дальнейшим превращениям — переносится на др. акцептор или восстанавливается.
Животные усваивают серу в составе органических соединений. Автотрофные организмы получают всю серу, содержащуюся в клетках, из неорганических соединений, главным образом в виде сульфатов. Способностью к автотрофному усвоению серы обладают высшие растения, многие водоросли, грибы и бактерии. (Из культуры бактерий был выделен специальный белок, осуществляющий перенос сульфата через клеточную мембрану из среды в клетку.) Большую роль в круговороте серы в природе играют микроорганизмы — десульфурирующие бактерии и серобактерии. Многие разрабатываемые месторождения серы — биогенного происхождения. Сера входит в состав антибиотиков (пенициллины, цефалоспорины); её соединения используются в качестве радиозащитных средств, средств защиты растений.
Л. И. Беленький.
Лит.: Справочник сернокислотчика, под ред. К. М. Малина, 2 изд., М., 1971; Природная сера, под ред. М. А. Менковского, М., 1972; Некрасов Б. В., Основы обшей химии, 3 изд., т. 1, М., 1973; Реми Г., Курс неорганической химии, пер. с нем., т. 1, М., 1972; Янг Л., Моу Д ж., Метаболизм соединений серы, пер. с англ., М., 1961; Горизонты биохимии, пер. с англ., М., 1964; Биохимия растений, пер. с англ., М., 1968, гл. 19; Торчинский Ю. М., Сульфгидрильные и дисульфидные группы белков, М., 1971; Дегли С., Никольсон Д., Метаболические пути, пер. с англ., М., 1973.