Альдегиды, класс органических соединений, содержащих карбонильную группу
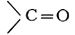 ,
,
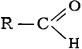
связанную c органическим радикалом (R) и с атомом водорода,
 .
.
Свойства альдегидов во многом сходны со свойствами кетонов, также содержащих карбонильную группу, но связанную с двумя радикалами, R2CO. Названия альдегидов обычно производят от названий соответствующих кислот. Так, муравьиной кислоте HCOOH соответствует муравьиный альдегид, или формальдегид HCHO; уксусной кислоте — уксусный альдегид, или ацетальдегид CH3CHO.
Из сопоставления формул спиртов RCH2OH, альдегидов RCHO и кислот RCOOH следует, что по степени окисленности альдегиды занимают промежуточное положение между этими соединениями. С этим связаны некоторые способы их получения и химические свойства. Так, при окислении первичных спиртов или при осторожном восстановлении хлорангидридов кислот образуются альдегиды:
RCH2OH + O ® RCHO + H2O;
RCOCI + H2 ® RCHO + HCI.
Промежуточному положению альдегидов отвечает и их способность к реакциям окисления-восстановления; например, в присутствии спиртового раствора едкой щёлочи альдегиды превращаются в смесь спирта и кислоты (см. Канниццаро реакция):
2C6H5CHO ® C6H5CH2OH + C6H5COOH.
Альдегиды могут быть получены также пиролизом смешанных кальциевых солей муравьиной и какой-либо другой карбоновой кислоты:
RCOOCaOOCH ® CaCO3 + RCHO.
Осторожным окислением ароматических соединений, содержащих метильную группу, получают ароматический альдегид.

Техническое значение имеет аналогичный способ получения простейшего ненасыщенного альдегида — акролеина — из пропилена:

Метод синтеза ацетальдегида, имеющий промышленное значение, состоит в гидратации ацетилена в присутствии солей ртути (см. Кучерова реакция):
HC º CH + H2O ® CH3CHO.
Альдегиды склонны к полимеризации; формальдегид, например, легко превращается в пара-формальдегид, ацетальдегид — в циклический тример, т. н. паральдегид. При конденсации 2 молей альдегидов образуются альдоли:
2CH3CHO ® CH3CH(OH)CH2CHO
(см. Альдольная конденсация), которые с отщеплением воды могут образовать ненасыщенные альдегиды:
CH3CH(OH)CH2CHO ® CH3CH = CHCHO + H2O
(см. Кротоновая конденсация).
Альдегиды легко вступают за счёт карбонильной группы во многие реакции присоединения и замещения. Так, с HCN они образуют циангидрины: RCH(OH)CN. Аналогично они реагируют с бисульфитом натрия, аминами и др. При действии гидроксиламина или гидразинов альдегиды дают соответственно оксимы RCH = NOH и гидразоны RCH = N—NH3.
Альдегиды широко применяют в производстве феноло-альдегидных смол, как душистые вещества (ванилин, цитраль и др.), как полупродукты синтеза др. веществ, например CH3CHO — для синтеза уксусной кислоты CH3COOH и этилацетата CH3COOC2H5 (см. Тищенко реакция), а также в синтезе олефинов и полиенов (см. Виттига реакция).
Я. Ф. Комиссаров.